 |
№ № 2–3 (35–36) 2024
Экологические особенности и биоразнообразие фототрофов карстовых пещер
Ecological features and biodiversity of phototrophic organisms in karst caves
Попкова А. В.
Anna V. Popkova
Российский университет дружбы народов имени Патриса Лумумбы (Москва, Россия)
УДК 574.589+574.24
Карстовые территории (пещеры) занимают 15–20% суши Земли, что делает их необычайно интересными и важными для исследований, но несмотря на это подземные полости представляют собой одни из наименее исследованных местообитаний на Земле. В обзоре приведены данные о специфике подземных местообитаний, а также об экологических особенностях и биоразнообразии фототрофов их экосистем. Описаны различные группы фототрофов, обитающие в пещерах. Обсуждаются механизмы адаптации фототрофных организмов к условиям подземных местообитаний, в том числе особенности фотосинтеза. Рассматриваются вопросы, связанные с влиянием экологических факторов, таких как температура, влажность, уровень фотонных потоков на распределение организмов в пещерах. Особое внимание уделено исследованиям входных зон и их биоты. Показано, что обособленность входных участков пещер позволяет рассматривать их как экотоны с особым набором параметров окружающей среды. Делается предположение, что зоны входов в пещеры могут выполнять функции рефугиумов, где способны обитать уникальные виды редких и исчезающих форм. Уделяется внимание проблемам миксотрофии представителей водорослей и цианобактерий, обитающих при слабом освещении либо в темноте. Отмечено, что в связи со значительным антропогенным изменением ландшафтов и сопутствующей этому процессу утратой местообитаний, пещерные ландшафты приобретают особую значимость.
Ключевые слова: карстовые пещеры; классификация пещер; биота карстовых пещер; экологические факторы карстовых пещер; фототрофы карстовых пещер; адаптация фототрофов к темноте
По некоторым оценкам, карстовые территории занимают 15–20% территории Земли (Ford, 2007; Engel, 2010). Пещеры находятся в различных регионах Земли и на всех широтах, но, как правило, они не взаимосвязаны между собой в глобальном масштабе. Подземные полости имеют самые разные формы и размеры, от микротрещин до пещер в несколько сот метров глубиной, и до сотен километров в длину. В глобальном масштабе исследовано около 10% всех пещер (Eavis, 2009; Engel, 2011).
Основанием научного интереса к экосистемам пещер является относительная географическая изоляция, недостаточность органических веществ, экстремальность условий подземных местообитаний, в том числе окислительно-восстановительных. Исследования пещер важны и с позиции формирования концепции о распространении биоты и эволюции экосистем в условиях темноты на планете Земля, а также обнаружения жизни в других частях Вселенной (Krajick, 2001; Forti, 2009).
Классификация и формирование пещер
Пещеры развиваются в растворимых породах. Различают карстовые (карбонатные породы, такие как известняк и доломит) и псевдокарстовые (некарбонатные породы) ландшафты. Наиболее распространенными являются известняковые пещеры. Менее распространены полости, заложенные в вулканических отложениях, гипсах, граните, кварците, песчанике, солях и льдах (Lee et al., 2012).
В данной работе карст понимается согласно определению А.С. Максимовича (1963): «Карст — это процесс химического и отчасти механического воздействия подземных и поверхностных внерусловых вод на растворимые проницаемые горные породы (карбонаты, гипс и ангидрит, соли, соду и другие). В результате возникают поверхностные, и подземные скульптурные, а при выпадении из раствора, обрушении — и аккумулятивные формы. Поглощенные трещинами, понорами, воронками, колодцами и шахтами воды, двигаясь в карстовом массиве, образуют различные подземные полости: пещеры, поддолинные (подрусловые) и другие каналы, каверны». Пещеры классифицируются согласно их генезису, типу породы, морфологии, обводненности, климатическим условиям (Palmer, 1991). В зависимости от близости к грунтовым водам, различают два типа пещер: эпигенные (образованные нисходящим процессом растворения горной породы водой, просачивающейся сверху) и гипогенные (образованные восходящими водами, в т.ч. насыщенными сероводородом и углекислотой, которые поднимаются из недр земли, растворяя горные породы изнутри) (Engel, 2011). Различные варианты процессов карстообразования и генезиса полостей, а также варианты типизации пещер рассмотрены в работе Hill, Forti (1986).
Подземные полости можно разделить на три размерных класса: микрокаверны (обычно <5 мм в ширину), мезокаверны (около 5–500 мм в ширину) и макрокаверны (пещеры >50 см в ширину) (Howarth, 1983). В настоящей работе будут исследованы макроковерны, т.е. пещеры.
Возраст большинства описанных и исследованных пещер составляет от тысяч до миллионов лет (Lee et al., 2012).
Специфика подземных местообитаний
В пещерах выделяют три зоны: входную, сумеречную и глубинную (deeper zone, deep cave – в англоязычной литературе). Данная классификация основывается, прежде всего, на световом факторе (Poulson, White, 1969; Northup, Lavoie, 2001). Во входную зону проникает солнечный свет, интенсивность которого зависит от дневного светового цикла. В сумеречную зону попадает частично прямой или отраженный солнечный свет. В глубинную зону свет не проникает (рис. 1).
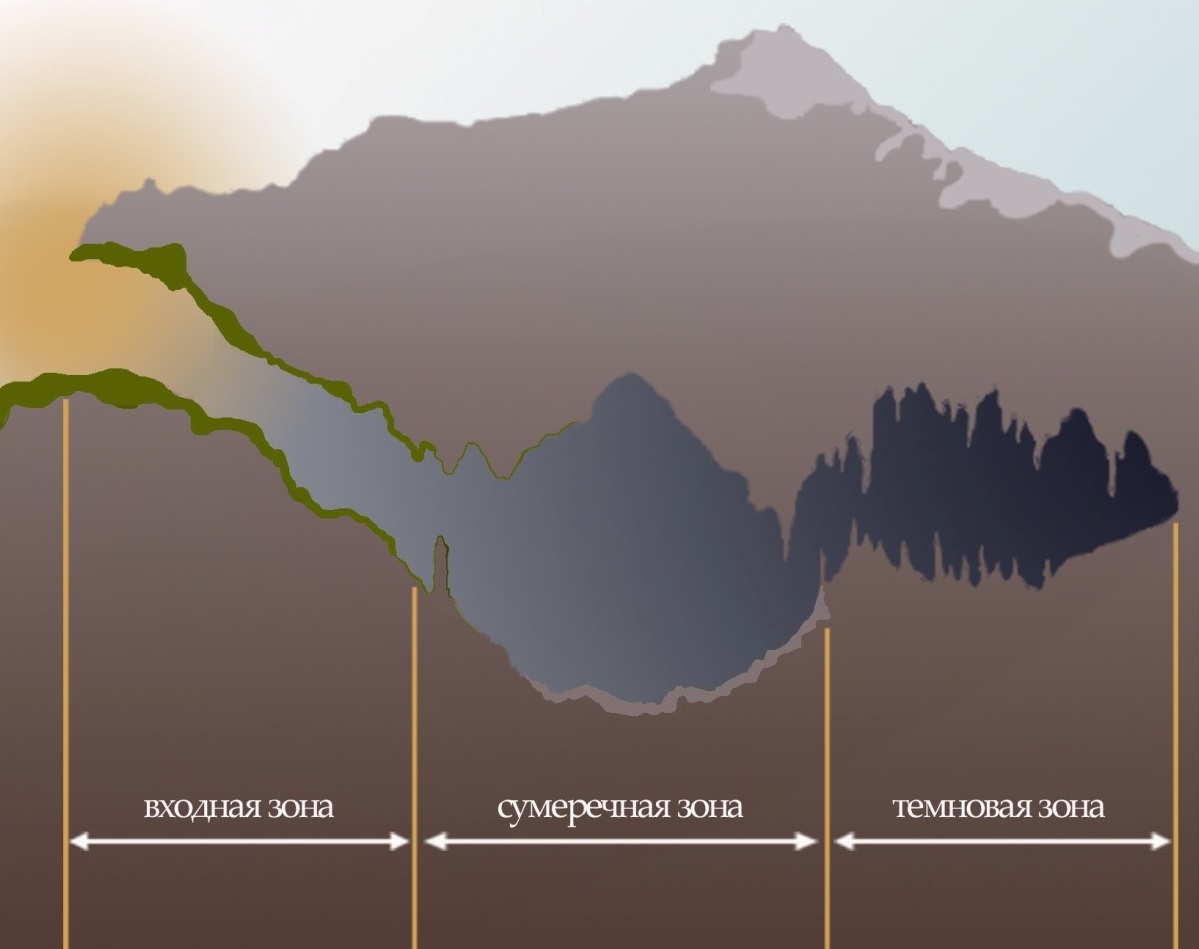
Рис. 1. Зонирование пещеры по световому фактору
Fig. 1. Light-based zoning of the cave
Для каждой зоны характерны специфические физико-химические условия: наличие источников освещения, температура, влажность, доступность воды, пористость и проницаемость субстрата, газовый состав атмосферы (табл. 1). Это влияет на потенциал колонизации и распространение живых организмов внутри пещеры (Bonacci et al., 2009).
Входная, сумеречная и темновая зоны имеют различный видовой состав биоты, который зависит от специфических физико-химических и геохимических условий, связанных, прежде всего, с фотохимическими градиентами и наличием органического вещества.
Таблица 1. Абиотические и биотические параметры, характерные для различных пещерных зон
Table 1. Abiotic and biotic parameters characteristic of different cave zones
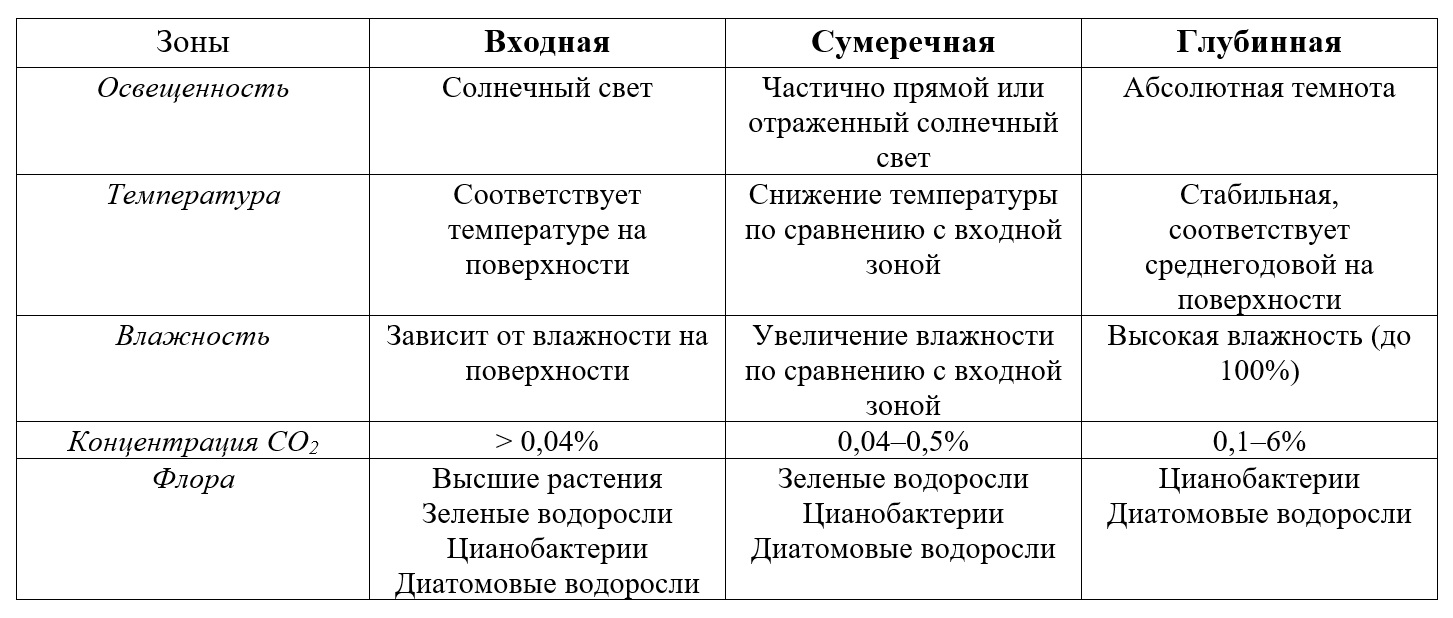
Условия и ресурсы пещер. Подземные карстовые полости рассматривают как климатически стабильные местообитания с низкими постоянными температурами, высокой относительной влажностью и низким уровнем световых потоков (Poulson, White, 1969). Отмечена зависимость температуры воздуха пещеры от аэротермической ступени, то есть при нахождении полости на более высоких отметках над уровнем моря понижается температура воздуха (Максимович, 1963). Для всех пещер наблюдается соответствие температуры воздуха в пещере среднегодовой температуре на поверхности (Максимович, 1963; Northup, Lavoie, 2001). Однако при наличии мощных водных потоков, имеющих отличную от пещерной температуру и привносящих теплые или холодные воды, соответственно изменяется температура воздуха в пещере. Температура пород и отложений в массиве является определяющей для температуры воздуха полости и определяется аналогичными критериями (Мазина и др., 2015).
Температура вод, поступающих в пещеру, зависит, прежде всего, от сезона. Холодные воды, воды снежников могут проникать в пещеру в том случае, если полость находится на горных территориях. Вода может просачиваться сквозь почву и породу по системе трещин, пор и каналов. При этом будет происходить ее нагрев. Чем более мощные потоки проникают в полость с поверхности и чем сильнее отличается их температура от температуры пещеры, тем больше вероятность того, что температура этих вод будет отличаться от температуры массива, в котором заложена пещера (Мазина, Семиколенных, 2015).
Влажность воздуха и субстратов в пещерах находится во взаимосвязи с поступающими в пещеру водами, что определяется как географическим положением пещеры, так и особенностями карстовых ландшафтов (Максимович, 1963). Для большинства карстовых пещер, заложенных в известняках и гипсах, характерна повышенная влажность, достигающая 100% (Czerwik-Marcinkowska, Mrozińska, 2011).
В карстовых массивах и пещерах отмечено движение воздуха, обусловленное, прежде всего, разностью плотностей двух столбов воздуха (рис. 2) – наружного поверхностного и подземного, или двух подземных столбов, или двух наружных (Максимович, 1963).
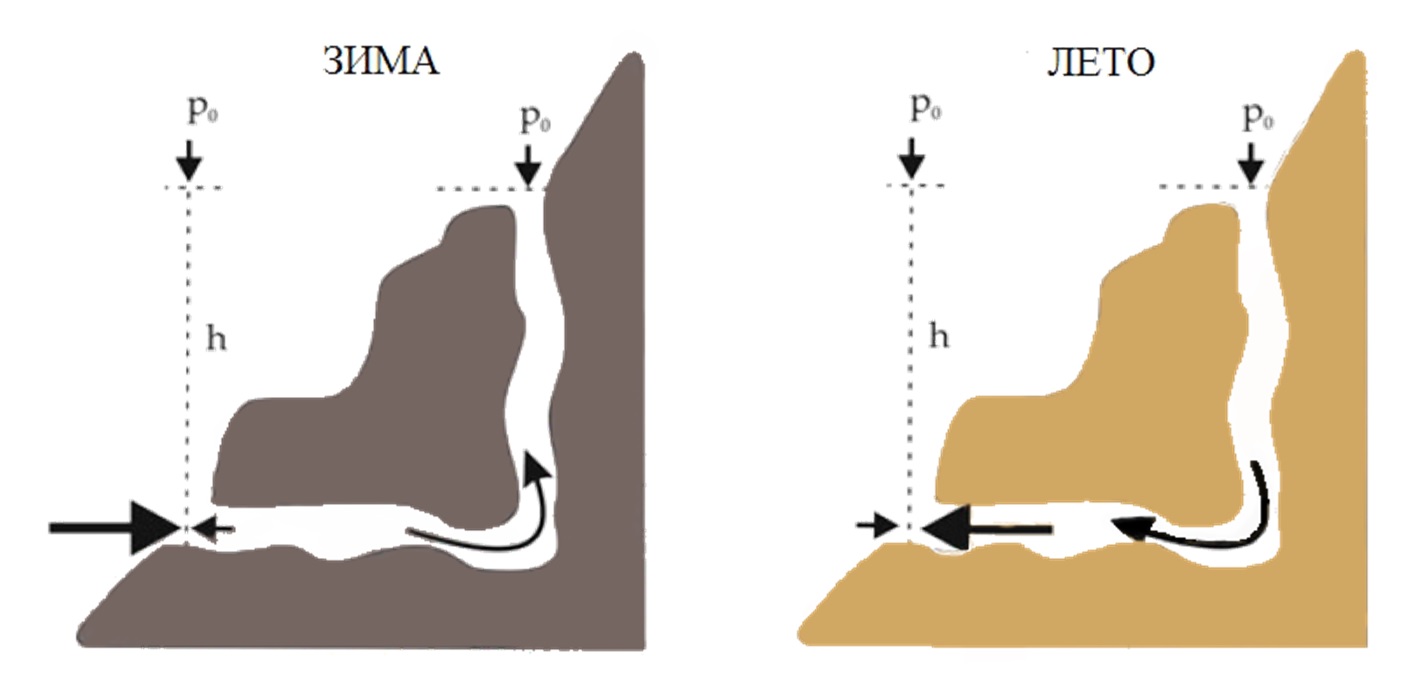
Рис. 2. Принцип движения воздуха на примере упрощенной модели пещеры
(по материалам Lauritzen, 2018)
Fig. 2. Air flow in a simplified cave model (after Lauritzen, 2018)
В воздухе карстовых пещер отмечается повышенная концентрация углекислого газа. Обычно концентрация СО2 в известняковых пещерах немного выше, чем на поверхности, находится на уровне 400–700 ppm, а в небольших полостях может быть и выше (Cowan et al., 2013). Источником поступления диоксида углерода в пещеру может быть как литогенный газ (гипогенное происхождение СО2), так и дыхание корней и почвенной биоты («почвенный газ», т.е. биогенное происхождение СО2). В работах Mandić et al., 2013 и Mattey et al., 2016 с использованием изотопного анализа СО2 и математического моделирования выявлена преимущественно биогенная природа углекислоты в изученных авторами пещерах. Это дало возможность с высокой долей вероятности предполагать, что небольшие полости, расположенные вблизи от поверхности, имеют повышенное содержание СО2 именно за счет близости растительности и биоты грунтов.
Определяющим фактором для развития сообществ является субстрат. Помимо вмещающей породы, в качестве субстрата могут выступать глинистые отложения различной толщины и увлажненности (Мазина, 2015). В подземных местообитаниях может быть отмечено образование почвоподобных тел. Согласно данным из работы А.А. Семиколенных, В.О. Таргульяна (2010): «в пещерах, где для поддержания продуктивности сообщества организмов химическая энергия используется вместо солнечной, формируются биокосные тела или системы, обладающие почвоподобной структурой (твердофазный каркас, профиль, горизонты) и функционально выполняющие роль почв на дневной поверхности, то есть оптимизирующие среду контакта биоты и минерального субстрата в процессе производства первичной биомассы».
В пещерах встречаются водные и вневодные местообитания. Вневодные местообитания представлены сводами пещер, вторичными минеральными образованиями и классифицируются в зависимости от влажности субстрата (степени обводненности субстрата). Водные местообитания (рис. 3) подразделяют на следующие группы: водные потоки различной динамики, капежи, т.е. просачивания воды в виде капель (временные, постоянные), лужи, ванночки (ванночки проточного типа, гуровые ванные), озера различной величины (проточные, могут быть заполняемыми с паводками, без постоянного притока) (Howarth, Moldovan, 2018).
Сообщества обрастаний пещер развиваются чаще всего в интерфейсах (местах стыковки двух систем). Например, в зоне между породой и воздухом (субаэральные сообщества) или в зоне между породой и водой (эпилитные сообщества обрастаний в водных потоках).
В подземных полостях реализуются 4 вида потоков:
- воздушные потоки – влияют на температуру воздуха и влажность;
- водные потоки – влияют на температуру воздуха и влажность, а также рельеф полости. С водными потоками в пещеру попадают зачатки видов, органические и минеральные вещества;
- потоки твердого вещества, которые перемещаются с током воздуха, воды или гравитационно (обвалы и т.д.);
- потоки с животными и человеком.
 Рис. 3. Водные местообитания в карстовых известняковых пещерах Рис. 3. Водные местообитания в карстовых известняковых пещерах
(по материалам Howarth, Moldovan, 2018)
Fig. 3. Water habitats in karst limestone caves (after Howarth, Moldovan, 2018)
Человек или животные привносят в пещеру органическое вещество, что увеличивает уровень трофности. В противном случае можно говорить об олиготрофности подземной среды, особенно в том случае, если пещера изолирована.
В некоторых неглубоких пещерах корни растений могут проникать в проходы и вносить аллохтонный органический углерод (Howarth, 1973). В глубинной зоне фотосинтез невозможен, поэтому в некоторых экосистемам в качестве источника энергии используется аллохтонный органический материал, полученный посредством ветра, проточной или капельной воды или гуано (Culver, Pipan 2009). Другие экосистемы используют автохтонный органический углерод, полученный в результате жизнедеятельности хемолитоавтотрофных микроорганизмов (Sarbu et al., 1996; Opsahl, Chanton 2006; Chen et al., 2009; Porter et al., 2009).
Экологические особенности и биоразнообразие фототрофов и микробиоты
подземных экосистем
Среди сообществ пещер выделяют эпилитные, развивающиеся на поверхности стен, сводов, натечных образований, сталактитах, сталагмитах (Roldán, Hernández-Mariné, 2009) и эндолитные сообщества. В случае эндолитных сообществ, микроорганизмы проникают вглубь субстрата (до нескольких миллиметров) (Golubic et al., 1981). В работах Gorbushina, Broughton (2009) и Albertano (2012) показано, что виды эпилитных и эндолитных сообществ являются литофилами, которые, как правило, устойчивы к стрессам и вариабельности условий среды
В состав подземных сообществ могут входить различные функциональные группы организмов: фототрофные цианопрокариоты, ассоциированные с микроводорослями, мхами, а также гетеротрофные бактерии и грибы. Подобные консорциумы часто обнаруживаются в форме биопленок, погруженных в экзополимерный матрикс, обеспечивающий адгезию к субстрату (Albertano, 2012). В состав экзополименого матрикса (EPS в англоязычной литературе) могут входить полисахариды, белки, липиды, нуклеиновые кислоты, неорганические вещества, которые объединяют в группу веществ. EPS способствуют поглощению ионов и регулируют процессы кальцификации, защищают биопленки от высыхания, токсических веществ и ультрафиолетового излучения (Bellezza et al., 2003, 2006; Albertano et al., 2005). Как следствие, EPS формируют тонкий липкий слой, богатый питательными веществами, который поддерживает высокий уровень влажности и делает биопленку устойчивой (Albertano, 1993). Анионная матрица EPS опосредуется межклеточной связью и участвует в обмене субстратами между членами сообщества (Hoffmann, 2002). Структура биопленки, как правило, связана с освещенностью: во входной зоне пещеры обычно наблюдается развитие толстых (обширных) биопленок с диатомовыми водорослями на поверхности. Толщина биопленок уменьшается пропорционально уменьшению освещенности (Hernández-Mariné et al., 2003; Roldán, Hernández Mariné, 2009; Zammit et al., 2011).
Фототрофы подземных карстовых полостей
По мнению Ivarsson et al. (2013), пещеры в целом являются неблагоприятными местообитаниями для фототрофных организмов, т.к. последние нуждаются в энергии фотонов для фотосинтеза. Однако в освещенной зоне входной части пещер или вокруг источников искусственного освещения в экскурсионных пещерах развиваются уникальные сообщества обрастаний, в основном состоящие из водорослей, цианобактерий, мхов, папоротников и иногда покрытосеменных. Выживание их в глубинных участках возможно лишь в случае изменения морфологической или морфофизиологической структуры, что рассматривается как экологические адаптации, тем самым ограничивая число видов, которые могут быть определены как подлинная «пещерная флора» (Racovitza, 1907).
Все виды, обитающие в пещерах, можно разделить на три группы (согласно Hoffmann, 2002):
- троглобионтные виды или облигатные подземные виды, которые не могут выжить вне пещеры;
- троглофитные виды, развивающиеся и размножающиеся в пещерах;
- троглоксентные виды, случайно попавшие в подземные карстовые полости.
Некоторые авторы считают, что к группе троглоксентных фототрофных организмов можно отнести диатомовые водоросли, которые попадают в подземную среду посредством циркуляции воздуха (Couté, Chauveau, 1994), либо с водными потоками (Kawecka, 1989).
К троглофитам относят цианобактерии Loriella osteophila Borzi, Scytonema julianum (Kützing) Meneghini Richter (Hoffmann, 2002). При этом вид S. julianum способен переносить резкие колебания условий среды (Ariño et al., 1997; Roldán, Hernández-Mariné, 2009), что объясняется способностью S. julianum осаждать карбонаты на своей оболочке (Albertano, Urzì, 1999).
Следует отметить, что троглобионтных видов крайне мало. К этой группе причисляют Geitleria calcarea Friedmann, G. floridana Friedmann, Herpyzonema pulverulentum Hernández-Mariné & Canals и Symphyonema cavernicolum Asencio, Aboal & Hoffmann (Lamprinou et al., 2009).
В зависимости от условий и ресурсов в различных зонах пещер могут быть выделены разные таксономические группы фототрофов.
Покрытосеменные обладают наименьшей толерантностью к низкому освещению (Dalby, 1966b). Как следствие, рост и развитие представителей отдела Magnoliophyta и Pteridophyta в подземных карстовых полостях наблюдается в основном в привходовых зонах, куда проникает прямой или отраженный свет (Martinič et al.,1981; Kubešová, 2001).
Наиболее часто встречаемой формой папоротников в подземных местообитаниях является заросток, который представляет собой развивающееся из споры половое поколение (гаметофит – гаплоидные структуры с многочисленными ризоидами внизу) (Kubešová, 2001; Mulec, Kubešová, 2010).
Бриофлора. Занос мохообразных в подземные полости осуществляется с поверхности – в виде пропагул (Rajczy, 1989; Šmarda, 1970). Как правило, преобладают виды, которые преимущественно населяют зону потенциального водосбора пещеры либо окрестности входа пещеры, а также производят большое количество спор либо способны к вегетативному размножению (Šmarda, 1970). В большинстве случаев мхи встречаются во входных частях пещер или в составе ламповой флоры. Однако, Koponen (1977) обнаружил мхи Ceratodon purpureus (Hedw.) Brid. и Pohlia nutans (Hedw.) Lindb. на глубине 176 м в шахте Виханти, Финляндия.
Большинство мхов пещер не являются специфичными для подземных местообитаний. Например, в результате исследований Reinoso et al. (1994) были выделены мхи, характерные для каньонов и расщелин, – Schistostega pennata (Hedw.) F.Weber & D.Mohr и Isopterygium elegans (Brid.) Lindb., а также лесные эпифиты – Diplophyllum albicans (L.) Dumort., Calypogeia arguta Nees et Mont., Calypogeia azurea Stotler et Crotz.
В некоторых случаях мхи в пещерах вовлечены в процесс литогенеза. Например, мхи Eucladium verticillatum (With.) Bruch et al. и Didymodon tophaceus (Brid.) Lisa участвовали в биокальцификации (Dalby, 1966а).
Наиболее часто встречаемыми видами мхов являются Amblystegium serpens (Hedw.) Bruch et al (Buczkó, Rajczy, 1989; Kubešová, 2001; Mulec, Kubešová, 2010), Fissidens taxifolius Hedw. (Conard, 1932; Thatcher,1949; Mulec, Kubešová, 2010; Мазина и др., 2015), туфообразующие Eucladium verticillatum (Dalby, 1966a; Komáromy et al., 1985; Buczkó, Rajczy, 1989; Mulec, Kubešová, 2010; Puglisi et al., 2019).
Часто мохообразные в пещерах встречаются в форме протонемы (Culver, Pipan, 2009; Мазина и др., 2015). По мнению Culver, Pipan (2009), для поддержания жизнедеятельности протонемы мхов необходимо меньше света, чем для водорослей и цианобактерий.
Мохообразные встречаются на таких субстратах как известняк, глина и натечные образования (Kubešová, 2001).
Водоросли и цианобактерии более толерантны к лимиту освещения (Шербэнеску, Деку, 1962) по сравнению с высшими растениями, что позволяет им проникать в отдаленные части пещер (Виноградова и др., 2009; Абдулин, 2014, 2015; Абдулин, Багмет, 2016; Козлова, 2021; Аллагуватова и др. 2022; Baković et al., 2022; Шарипова, Дубовик, 2024).
Во многих регионах мира детально изучен таксономический состав водорослей и цианобактерий входных участков пещер (Claus, 1955; Kol, 1964; Cox et al, 1989; Buczkó, Rajczy, 1989; Klemenič, Vrhovšek, 2005; Selvi, Altuner, 2007; Виноградова и др., 2000; Абдуллин, Шарипова, 2005; Lauriol et al, 2006; Виноградова и др., 2009; Виноградова, Михайлюк, 2009; Абдуллин, 2009; Lamprinou et al., 2009; Martinez, Asencio, 2010; Czerwik-Marcinkowska, Mrozińska, 2011; Czerwik-Marcinkowska, 2013; Lamprinou et al., 2012; Popović et al., 2015), а также сообществ ламповой флоры (Smith, Olson, 2007; Мазина, 2009; Mulec, Kosi, 2009; Мазина, Максимов, 2011, Cennamo et al., 2012; Lamprinou et al., 2014; Мазина и др., 2015; Pfendler et al., 2018; Козлова, 2021).
Отмечено доминирование в сообществах представителей родов зеленых водорослей: Chlorella, Mychonastes, Chlorococcus и цианобактерий: Chroococcus, Microcystis, Nostoc, Leptolyngbya. Вышеуказанные организмы хорошо приспособлены к недостаточному освещению и как следствие способны колонизировать широкий спектр субстратов (Macedo et al., 2009).
В зонах с низкой освещенностью, как правило, доминантами среди фототрофов являются цианобактерии, первые фотосинтезирующие колонизаторы многих субстратов на поверхности (Albertano, 1999; Whitton, Potts, 2000; Smith, Olson, 2007; Lamprinou et al., 2009).
Например, цианобактерия Gloeocapsa punctata широко распространена в Европе и была выявлена в сообществах фототрофов пещер в Сербии (Popović et al., 2015), Украине (Виноградова, Михайлюк, 2009), Чехии (Poulíčková, Hašler, 2007), Словении (Ettl, Gärtner, 1995; Mulec, Kosi, 2008), Словакии (Uher, Kováčik, 2002), Венгрии (Kol, 1964; Buczko, Rajczy, 1989), Великобритании (Pentecost, Zhaohui, 2001).
Обсуждается вклад цианобактерий в генезис сложных микробных сообществ. Отмечено, что выработка внеклеточных полимерных веществ (Stal, 2000; Cennamo et al., 2012), способность к фиксации атмосферного азота цианобактериями (Lamprinou et al., 2012) содействует созданию благоприятных условий для развития других организмов (не способных к азотфиксации цианобактерий, водорослей, мхов и т.д.).
На натечных образованиях и стенах пещер вследствие конденсации влаги развиваются диатомовые водоросли (Kol, 1957; Dobat, 1970; Lauriol. et al., 2006; Mulec, Kosi, 2009). Биоразнообразие диатомовых водорослей обычно связано с удаленностью от входной зоны пещеры. Лиминарная (Liminar zone, т.е. участок от входа в пещеру до глубины, где освещенность снижается до 50% от внешней интенсивности света) и сублиминарная (Subliminar zone, т.е. следующая, более глубокая зона, где освещенность составляет менее 50% от внешней интенсивности света) зоны пещер обычно характеризуются высоким видовым богатством диатомовых водорослей, вероятно, в зависимости от влияния внешних условий и их суточных и сезонных колебаний (Hoffmann, 2002; Roldán et al., 2004; Mulec et al., 2008).
Изменения в составе диатомовых водорослей и их обилии связаны с освещенностью (Patrick, 1948) и колебаниями влажности, но невозможно исключить роль когерентности субстрата и межвидовой конкуренции (Roldán et al., 2004). Как правило, влажные и освещенные поверхности со значительным присутствием мхов более богаты диатомовыми водорослями, чем менее освещенные и сухие участки (St. Clair et al., 1981; Altieri et al., 1993). Влажные участки, как правило, колонизированы Nitzschia sp. и Pinnularia borealis Ehrenberg (Czerwik-Marcinkowska, Mrozińska, 2009). Мхи и папоротники могут содержать на своей поверхности популяции Humidophila gallica (W.Smith) Lowe, Kociolek, Q.You, Q.Wang & Stepanek и Orthoseira roeseana (Rabenhorst) Pfitzer (Roldán, Hernández-Mariné, 2009). Hantzschia amphioxys (Ehrenberg) Grunow, Luticola mutica (Kützing) D.G.Mann и Pinnularia borealis также являются распространенными эпифитами (Poulíčková, Hašler, 2007). Химический состав породы влияет на состав и разнообразие сообщества диатомовых водорослей. pH также формирует видовой состав сообществ: например, Humidophila gallica и Humidophila laevissima P.T.Cleve) Lowe, Kociolek, Johansen, Van de Vijver, Lange-Bertalot & Kopalová выявлены в нейтрально-щелочных пещерах, в то время как Humidophila contenta Grunow) Lowe, Kociolek, J.R.Johansen, Van de Vijver, Lange-Bertalot & Kopalová и Eunotia exigua (Brébisson ex Kützing) Rabenhorst обнаружены в кислотных просачиваниях (Poulíčková, Hašler, 2007). Согласно Selvi, Altuner (2007) в некоторых пещерах низкое биоразнообразие диатомей можно объяснить лимитированным содержанием кремния.
Анализ данных литературы показывает, что наиболее часто встречаемыми видами диатомовых водорослей являются Hantzschia amphioxys, Humidophila contenta, Orthoseira roeseana, Luticola nivalis (Ehrenberg) D.G.Mann, Pinnularia borealis, Diadesmis contenta var. biceps (Grunow) P.B.Hamilton in Hamilton & al. и Luticola mutica (Falasco et al., 2014). Все эти виды являются аэрофилами, могут развиваться в почвах (Petersen, 1928; Lund, 1946; Bock, 1963; Ettl, Gärtner, 1995; Souffreau et al., 2010). С экологической точки зрения они, как правило, являются эврибионтами и могут размножаться в различных условиях окружающей среды (Falasco et al., 2014).
Диатомовые водоросли исследованы во многих пещерах мира (Claus, 1955; Kol, 1957; Palik, 1960; Dobat, 1970; Carter, 1971; St.Clair, Rushforth, 1976; Bahls, 1981; St.Clair et al. 1981; Kashima et al.,1987; Dayner, Johansen, 1991; Buczkó, Rajczy, 1989; Garbacki et al., 1999; Buczkó, 2003; Lauriol et al., 2006; Poulíčková, Hašler, 2007; Czerwik-Marcinkowska, Mrozińska, 2009, 2011; Виноградова, Михайлюк, 2009; Аллагуватова, 2022). Однако в основном эти работы были посвящены изучению таксономического состава, а не экофизиологических характеристик видов.
Адаптации фототрофных организмов к условиям подземных местообитаний
Важным направлением экологических исследований является определение механизмов адаптации фототрофных организмов к условиям подземных местообитаний (Golubić, 1967; Couté, 1982; Aboal et al., 1994; Couté, Chauveau, 1994; Hernández-Mariné et al., 1999; Giordano et al., 2000; Whitton, Potts, 2000; Hoffmann, 2002; Mulec et al., 2008).
Показано, что возможны следующие варианты адаптаций фототрофных организмов к условиям подземных местообитаний.
Морфологические и физиологические адаптации. Есть мнение, что коккоидная форма клеток лучше приспособлена к низкому уровню фотонов по сравнению с другими формами цианобактерий (Mulec et al., 2008).
Обсуждается роль внеклеточных оболочек в адаптации цианобактерий. Предполагается, что помимо адгезии к субстрату, внеклеточная оболочка выступает в качестве резервуара для воды, что позволяет цианобактериям выжить в периоды засухи (Macedo et al., 2009; Keshari, Adhikary, 2013). Кроме полисахаридов во внеклеточных оболочках обнаружены гликаны, УФ-абсорбирующие пигменты, белки водного стресса (Pattanaik et al., 2007).
Отмечено, что некоторые водоросли, которые обитают в известняковых пещерах, осаждают кристаллы карбоната кальция (CaCO3) на клеточной оболочке. Например, цианобактерии рода Scytonema имеют кальцинированные трихомы. Такое явление наблюдалось в пещерных зонах с низкой интенсивностью света. Показано, что организмы с кальцинированными трихомами выживают лучше, чем те, у которых нет отложений CaCO3 (Lamprinou et al., 2012).
Исследования ультраструктуры представителей родов Chroococcidiopsis, Cyanosarcina, Leptolyngbya, Phormidium и Pseudocapsa, выделенных из пещер в Мурсии, Испания (Asencio, Aboal, 2004), свидетельствуют о хорошо развитой системе тилакоидов и о наличии всех наиболее широко известных клеточных включений (карбоксисомы, гранулы гликогена и цианофицина, липиды, глобулы, полифосфатные и полибутилоксимасляные тела).
Была отмечена фототаксическая активность и наличие светоулавливающих глазков, состоящих из каротиноидных глобул и родопсина (Albertano et al. 2000), у штамма VRUC 135 Leptolyngbya, позже описанного как Oculatella subterranea gen. Nov., Sp. Nov (Zammit et al., 2012). Эта сложная фоторецептивная структура может иметь эволюционное значение, поскольку она напоминает хлоропласт зеленых жгутиконосцев.
Описаны различные физиологические адаптации, связанные с недостаточным уровнем фотонных потоков: инициация стадий покоя у диатомовых (Sicko-Goad et al., 1989; McQuoid, Hobson, 1996), формирование цист у динофитовых водорослей (Dale, 1983; Chapman, Pfiester, 1995; Rengefors, Anderson, 1998) и акинет (покоящиеся клетки с утолщенной оболочкой, большим количеством запасных питательных веществ и пигментов) у цианобактерий (Rother, Fay, 1977; Li et al., 1997).
Модификации в фотосинтетическом аппарате. Описаны изменения количества пигментов и ассоциированных с ними пигментобразующих белков в ответ на изменение уровня освещенности (Yentsch, Reichert, 1963; Bunt, Lee, 1972; Tilzer et al., 1977; Murphy, Cowles, 1997; Luder et al., 2002). Например, снижение плотности потока фотонов почти всегда приводит к увеличению концентрации хлорофилла а (Miskiewicz et al., 2000; MacIntyre et al., 2002) и фикобилинов (Grossman et al., 1994; Mulec et al., 2008). Для зеленых водорослей типичное отношение хлорофилла а к хлорофиллу b составляет 3:1 при 100 мкмоль м-2 с-1 (Kirk, 1983).
Отмечена способность клеток синтезировать вспомогательные фотосинтезирующие пигменты для захвата большего количества доступных фотонов при низкой освещенности (Macedo et al., 2009; Martinez, Asencio, 2010).
Биопленки, в состав которых входят представители рода Gloeocapsa, имеют самые различные окраски из-за наличия пигмента глоекапсина. Другой хорошо изученный пигмент сцитонемин вызывает темную окраску цианобактериального мата. Этот желто-коричневый пигмент представляет собой один из УФ-поглощающих компонентов, которые скапливаются во внеклеточной оболочке цианобактерий при воздействии солнечной радиации (Balskus, Walsh, 2008). Преобладание темного окрашивания обычно наблюдается у родов Scytonema, Nostoc и Tolypothrix (Pattanaik et al., 2007).
Исследования показали, что интенсивность фотосинтеза может служить индикатором степени устойчивости к стрессу, особенно для одноклеточных водорослей (Young, Beardall, 2003). Типичные кривые фотосинтеза для водорослей, адаптированных к условиям низкой освещенности, характеризуются высокой эффективностью фотосинтеза, низкой фотосинтетической емкостью, а также фотоингибированием фотосинтеза уже при достаточно низком уровне излучения (Falkowski, La Roche, 1991; Kirst, Wiencke, 1995).
Миксотрофия. Большинство микроводорослей и цианобактерий являются облигатными фототрофами. Однако в периоды низкой освещенности некоторые цианобактерии и микроводоросли способны переходить на гетеротрофное питание. Это обеспечивает долгосрочное сохранение жизнеспособности (Adhikary, 2002).
Миксотрофия является объектом исследования различных научных направлений. С точки зрения экологии, миксотрофия – это метаболическая стратегия некоторых организмов, объединяющая в себе черты авто- и гетеротрофии, то есть использование различных источников углерода и энергии (Jones, 1994, 2000). C точки зрения цитофизиологии, миксотрофия – это комплексный тип метаболизма.
Миксотрофный рост представляется весьма энергозатратным, и организм всегда должен поддерживать оптимальный баланс физиологических затрат и выгод. С одной стороны, клетке необходимо поддерживать фотосинтетический аппарат и весь набор ферментов цикла Кальвина, необходимый для фотосинтеза и фиксации неорганического углерода. С другой стороны, для гетеротрофного роста нужны мембранные транспортеры простых органических веществ, зачастую экто- и экзоферменты для внеклеточного гидролиза органических полимеров (Матанцева, Скарлатто, 2013).
Следует отметить, что гетеротрофное культивирование фототрофов может быть хорошо контролируемым и обеспечивает возможность достижения быстрого роста и высокого выхода ценных продуктов в больших масштабах, что может быть полезным для целей биотехнологии (Горбунова, Жондарева, 2017; Жондарева, Тренкеншу, 2024). Существует несколько стратегий для культивирования фототрофных микроорганизмов без света (Chen, Chen, 2006). Исследования доказали, что миксотрофия может быть потенциальным механизмом снижения затрат на культивирование микроводорослей (Smith et al., 2020). Миксотрофное культивирование имеет существенные преимущества перед фототрофным культивированием микроводорослей: теоретически более низкая стоимость (Perez-Garcia et al., 2011), повышенное количество биомассы (Day, Tsavalos, 1996), повышенная плотность клеток (Kumar et al., 2018) и увеличение целевого биохимического компонента (Pahl et al., 2010). Таким образом, выделение уникальных потенциально миксотрофных видов может быть перспективным направлением исследований.
Мискотрофия была описана для ряда фототрофных видов, обитающих в карстовых пещерах (Chen, Chen, 2006), в том числе для широко распространенной в пещерах Leptolyngbya boryana (Gomont) Anagnostidis & Komárek (Raboy, Padan, 1978). Показано использование экзогенных сахаров для гетеротрофного и фотогетеротрофного роста Scytonema coactile Montagne ex Bornet & Flahault, выделенной из сумеречной зоны одной из индийских пещер. Эксперимент проходил при разных световых режимах (Lakshmi et al., 2008).
Заключение
На основании рассмотренных исследований можно констатировать, что таксономический состав и структура сообществ микробиоты подземных полостей достаточно неплохо изучены во многих странах мира, однако есть регионы, в которых подобные исследования не проводились. Обособленность входных участков пещер, рассматриваемых как экотоны, и уникальность параметров их среды, в которой развиваются в том числе фототрофы, делают важным изучение биоразнообразия этих местообитаний для понимания биоразнообразия регионов в целом и локальных флор в частности.
Анализ исследований показывает, что на видовой состав микробиоты подземных полостей и распределение организмов в пещерах оказывают влияние различные экологические факторы, такие как температура, влажность, освещенность и др. Однако остаются открытыми вопросы об экологических нишах, межвидовых взаимодействиях в сообществах пещер, а также адаптивных возможностях и пределах толерантности видов, обитающих в подземных полостях.
Зоны входов пещер могут выполнять функции рефугиумов, то есть можно ожидать нахождение в этих местах уникальных видов, редких и исчезающих форм. В связи со значительным антропогенным изменением ландшафтов и сопутствующей этому процессу утратой местообитаний, стабильные и слабо трансформируемые пещерные ландшафты приобретают особую значимость. В то же время и сами пещеры подвержены антропогенному воздействию, которое может быть как опосредованным, связанным с общим изменением биосферы, так и локальным, в том случае при хозяйственном использовании пещер или развитии спелеотуризма. Хозяйственная деятельность оказывает влияние на все компоненты экосистем пещер в пределах карстового массива, где расположена пещера. Что касается непосредственно входной зоны, то ее переустройство, связанное с переоборудованием входа или возрастанием потока посетителей, наиболее разрушительно для сообществ обрастаний.
Учитывая важную роль карстовых массивов в формировании и сохранении подземных вод, а также тот факт, что входы пещер связывают поверхностные и подземные ландшафты, особую значимость приобретает исследование входных зон и их биоты.
Автор заявляет об отсутствии конфликта интересов, требующего раскрытия в данной статье.
Список литературы
- Абдуллин Ш.Р. Биоразнообразие цианобактерий и водорослей Аскинской пещеры (Южный Урал) // Вестник ОГУ. 2009. №6. С. 9–10.
- Абдуллин Ш.Р. Разнообразие трофической структуры экосистем пещер // Успехи современной биологии. 2014. Т. 134, №2. С. 192–204.
- Абдуллин Ш.Р. Закономерности формирования разнообразия и таксономия цианобактериально-водорослевых ценозов пещер России и некоторых сопредельных государств: дис. д-ра биол.наук. Уфа: Башкирский государственный университет, 2015. 440 с.
- Абдуллин Ш.Р., Багмет В.Б. Миксотрофия цианобактерий и водорослей в условиях пещер // Журнал общей биологии. 2016. Т. 77, № 1. С. 54–62.
- Абдуллин Ш.Р., Шарипова М.Ю. Альгофлора пещеры Шульган-Таш (Каповой) в различные годы // Вестник Башкирского университета. 2005. №3. С. 49–50.
- Аллагуватова Р.З., Никулин А.Ю., Багмет В.Б., Абдуллин Ш.Р. Биоразнообразие цианобактерий и водорослей пирокластических отложений и почв вулканов юга Камчатки // Вестник ДВО РАН. 2022. №5. С. 75–87. DOI: http://doi.org/10.37102/0869-7698_2022_225_05_6
- Виноградова О.Н., Коваленко О.В., Вассер С.П., Нево Э.Д., Вайнштейн-Эврон М. Синезеленые водоросли (Cyanoprocaryota) пещеры Джамал (Национальный парк Маунт Кармель, Израиль) // Альгология. 2000. Т.10, №1. С. 82–90.
- Виноградова О.Н., Михайлюк Т.И. Альгофлора пещер и гротов национального природного парка «Подольские Товтры» (Украина) // Альгология. 2009. Т.19, № 2. C. 155–171.
- Виноградова О.Н., Нево Э., Вассер C.В. Альгофлора пещеры Сефуним (Израиль): видовое разнообразие в условиях мультифакторного абиотического стресса // Альгология. 2009. Т. 19. № 1. C. 47–65.
- Горбунова С.Ю., Жондарева Я.Д. Миксотрофное питание как пример экологически приемлемой технологии для культивирования цианобактерии Arthrospira (Spirulina) platensis (Nordst) Geitler // Вопросы современной альгологии. 2017. № 2 (14). URL: http://algology.ru/1176 (дата обращения: 10.02.2024)
- Жондарева Я.Д., Тренкеншу Р.П. Миксотрофный рост Tetraselmis viridis в аксенической накопительной культуре // Вопросы современной альгологии. 2024. №1(24). С. 21–28. URL: http://algology.ru/2097. (дата обращения: 10.02.2024) DOI: https://doi.org/10.33624/2311-0147-2024-1(34)-21-28; END: MULCZK
- Козлова Е.В. Структурно-функциональные особенности сообществ входных зон карстовых пещер Черногории. Дисс. к- та биол. наук. М.: 2021. – 221с.
- Мазина С.Е. Ламповая флора Новоафонской пещеры // Политематический сетевой электронный научный журнал Кубанского государственного аграрного университета. 2015. Т. 9. № 113. C. 1–12.
- Мазина С.Е. Сообщества фотосинтезирующих организмов, развивающихся в условиях искусственного освещения на оборудованном участке пещеры Мраморная // Спелеология и Карстология. 2009. №2. С. 92–99.
- Мазина С.Е., Концевова А.А., Юзбеков А.К. Фотосинтезирующие виды пещеры Новоафонская, развивающиеся в условиях искусственного освещения // Естественные и технические науки. 2015. Т.88, №10. С. 162–171.
- Мазина С.Е., Максимов В.Н. Сообщества фотосинтезирующих организмов экскурсионной пещеры Ахштырская // Вестн. Моск. ун-та. Сер. 16. Биология. 2011. № 1. С. 41–46.
- Мазина С.Е., Семиколенных А.А. Формирование почвоподобных тел на участках искусственного освещения в пещерах // Материалы докладов международной научной конференции. Роль почв в биосфере и жизни человека. К 100-летию со дня рождения академика Г.В. Добровольского, к Международному году почв. – М.: МАКС Пресс, 2015. – С. 205–207.
- Максимович Г.А. Основы карстоведения. Вопросы морфологии карста, спелеологии и гидрогеологии карста. – Пермь: Пермское Книжное Издательство, 1963. – Т.1. – 445 с.
- Матанцева О.В., Скарлато С.О. Миксотрофия у микроорганизмов: экологические и цитофизиологические аспекты // Журнал эволюционной биохимии и физиологии. 2013. Т. 49, № 4. С. 245–254.
- Семиколенных А.А., Таргульян В.О. Почвоподобные тела автохемолитотрофных экосистем пещер хребта Кугитангтау (Восточный Туркменистан) // Почвоведение. 2010. № 6. С. 658–672.
- Шарипова М.Ю., Дубовик И.Е. Цианобактерии и водоросли Карламанской пещеры (Республика Башкортостан, Россия) // Теорeтическая и прикладная экология. 2024. № 1. С. 184-190. DOI: 10.25750/1995-4301-2024-1-184-190
- Шербэнеску М., Деку В. К изучению пещерных водорослей Олтении // Rev. Biol. 1962. Т.7, №2. C. 201–214.
- Aboal M., Asencio A.D., Prefasi M. Studies on cave cyanophytes from southeastern Spain: Scytonema julianum (Meneghini ex Franck) Richter // Algological Studies Arch Hydrobiol Suppl. 1994. V.75. P. 31–36. DOI: https://doi.org/10.1127/algol_stud/75/1995/31
- Adhikary S.P. Survival in darkness and heterotrophic growth of epilithic cyanobacteria from temples of India // Algological Studies Arch Hydrobiol Suppl. 2002. V.105. P. 141–155. DOI: https://doi.org/10.1127/algol_stud/105/2002/141
- Albertano P. Cyanobacterial biofilms in monuments and caves // B.A. Whitton (Ed.), Ecology of Cyanobacteria II: Their Diversity in Space and Time. – Springer Dordrecht, Springer Science+Business Media B.V., 2012. P. 317–345. DOI: https://doi.org/10.1007/978-94-007-3855-3
- Albertano P. Epilithic algal communities in hypogean environments // Giornale Botanico Italiano. 1993. V.127. P. 386–392. DOI: http://doi.org/10.1080/11263509309431020
- Albertano P., Bruno L., Bellezza S. New strategies for the monitoring and control of cyanobacterial films on valuable lithic faces // Plant Biosystems. 2005. V.139. P. 311–322. http://doi.org/10.1080/11263500500342256
- Albertano P., Urzí C. Structural interactions among epilithic Cyanobacteria and heterotrophic Microorganisms in Roman Hypogea // Microbial ecology. 1999. V.38. P. 244–252. DOI: http://doi.org/10.1007/s002489900174
- Albertano P., Barsanti L., Passarelli V., Gualtieri P. A complex photoreceptive structure in the cyanobacterium Leptolyngbya sp. // Micron. 2000. V.31. P. 27–34. DOI: https://doi.org/10.1016/S0968-4328(99)00063-3
- Altieri A., Pietrini A.M., Ricci S. Un’associazione di alghe e muschi in un sito archeologico ipogeo // Giornale Botanico Italiano. 1993. V.127. P. 611.
- Ariño X., Hernández-Mariné M., Saiz-Jimenez C. Colonization of Roman tombs by calcifying cyanobacteria // Phycologia. 1997. V.36. P. 366–373.
- Asencio A.D., Aboal M. Cell inclusions in the chasmoendolithic Cyanophytes from cave-like environments in Murcia (SE Spain) // Algological Studies Arch Hydrobiol Suppl. 2004. V. 113. P. 117–127. DOI: https://doi.org/10.1127/1864-1318/2004/0113-0117
- Bahls L.L. Diatoms of Lewis and Clark Caverns // Proceedings of the Montana Academy of Sciences. 1981. V.40. P.11–18.
- Baković N., Pipan T., Baković R., Ozimec R., Rubinić J., Matoničkin Kepčija R. Algae and cyanobacteria in the aphotic habitats of Veternica Cave (Medvednica Mt., Croatia) and selected caves of the Dinaric karst (Southeast Europe) // International Journal of Speleology. 2022. V. 51(3). P. 193–203. DOI: https://doi.org/10.5038/1827-806X.51.3.2422
- Balskus E.P., Walsh C.T. Investigating the initial steps in the biosynthesis of cyanobacterial sunscreen scytonemin // Journal of the Chemical American Society. 2008. V.130, № 46. P. 15260–15261. DOI: https://doi.org/10.1021/ja807192u
- Bellezza S., Albertano P., de Philippis R., Paradossi G. Exopolysaccharides of two cyanobacterial strains from Roman hypogeal // Geomicrobiology Journal. 2006. V.23. P. 301–310. DOI: https://doi.org/10.1080/01490450600761904
- Bellezza S., Paradossi G., De Philippis R., Albertano P. Leptolyngbya strains from Roman hypogea: cytochemical and physico-chemical characterisation of exopolysaccharides // Journal of Applied Phycology. 2003. V.15. P. 193–200. DOI: https://doi.org/10.1023/A:1023811311686
- Bock W. Diatomeen extrem trockener Standorte // Nova Hedwigia. 1963. V.5. P. 99–254.
- Bonacci O., Pipan T., Culver D.C. A framework for karst ecohydrology // Environ Geol. 2009. V.56. P. 891–900. DOI: https://doi.org/10.1007/s00254-008-1189-0
- Buczkó K. Diadesmis brekkaensoides (W. Bock) Moser, Lang.e-Bertalot et Metzeltin: a new aerophytic diatom for the Hungarian flora // Studia Botanica Hungarica. 2003. V.34. P. 5–10.
- Buczkó K., Rajczy M. Contributions to the flora of the Hungarian caves II. Flora of the three caves near Beremend, Hungary // Studia Botanica Hungarica. (Antea: Fragmenta Botanica). 1989. V.21. P. 13–25.
- Bunt J.S., Lee C.C. Data on the composition and dark survival of four sea-ice microalgae // Limnology & Oceanography. 1972. V.17. P. 458–462. DOI: https://doi.org/10.4319/lo.1972.17.3.0458. DOI: https://doi.org/10.4319/lo.1972.17.3.0458
- Carter J.R. Diatoms from the Devil’s Hole Cave Fife, Scotland // Nova Hedwigia. 1971. V.21. P. 657–681.
- Cennamo P., Marzano C., Ciniglia C., Pinto G., Cappelletti P., Caputo P., Pollio A. A survey of the algal flora of anthropogenic caves of Campi Flegrei (Naples, Italy) archeological district // Journal of Cave and Karst Studies. 2012. V.74, №3. P. 243–250. DOI: 10.4311/2011JCKS0194
- Chapman A.D., Pfiester L.A. The effects of temperature, irradiance, and nitrogen on the encystment and growth of the freshwater dinoflagellates Peridinium cinctum and Peridinium willei in culture (Dinophyceae) // Journal of Phycology. 1995. V. 31. P. 355–359.
- Chen G.Q., Chen F. Growing phototrophic cells without light // Biotechnology Letters. 2006. V. 28. P. 607–616. DOI: https://doi.org/10.1007/s10529-006-0025-4
- Chen Y., Wu L., Boden R., Hillebrand A., Kumaresan D., Moussard H., Baciu M., Lu Y., Murrell J.C. Life without light: microbial diversity and evidence of sulfur- and ammonium-based chemolithotrophy in Movile Cave // ISME J. 2009. V.3. P. 1093–1104. DOI: https://doi.org/10.1038/ismej.2009.57
- Chodat R. Étude critique et expérimentale sur le polymorphisme des algues. – Genève: Georg & Cie, 1909. – 165 p.
- Claus G. Algae and their mode of life in the Baradla cave at Aggtelek // Act. Bot. Acad. Sc. Hungar. 1955. V.2, №1–2. P. 1–26.
- Conard H.S. Cave mosses // Bryologist. 1932. 13 p.
- Couté A., Chauveau O. Algae // Encyclopaedia Biospeologica 1. Eds.: Juberthie C. & Decu V. – Société de Biospéléologie, Moulis–Bucarest, 1994. – P. 371–380.
- Couté A. Ultrastructure d'une cyanophycée aérienne calcifiée cavernicole: Geitleria calcarea Friedmann // Hydrobiologia. 1982. V.97. P. 255–274. DOI: https://doi.org/10.1007/BF00007113
- Cowan B.D., Osborne M.C., Banner J.L. Temporal variability of cave-air CO2 in central Texas // Journal of Cave and Karst Studies. 2013. V.75, №1. P. 38–50. DOI: 10.4311/2011ES0246
- Cox G., James J.M., Leggett K.E.A., Osborne R.A.L. Cyanobacterially deposited speleothems: Subaerial stromatolites // Geomicrobiology J. 1989. V.7. Р. 245–252.
- Culver D.C., Pipan T. The biology of caves and other subterranean habitats. – Oxford University Press, 2009. – P. 1−273.
- Czerwik-Marcinkowska J. Observations on aerophytic cyanobacteria and algae from ten caves in the Ojców national park // Acta Agrobotanica. 2013. V.66, №1. P.39–52. DOI: https://doi.org/10.5586/aa.2013.005
- Czerwik-Marcinkowska J., Mrozińska T. Algae and cyanobacteria in caves of the Polish Jura // Polish Botanical Journal. 2011. V.56, №2. P. 203–243. (In Polish)
- Czerwik-Marcinkowska J., Mrozińska T. Epilithic algae from caves of the Krakowsko-Czestochowska upland (Southern Poland) // Acta Societatis Botanicorum Poloniae. 2009. V.78, №4. P. 301–309. DOI: https://doi.org/10.5586/asbp.2009.040
- Dalby D.H. The growth of Eucladium verticillatum in a poorly illuminated cave // Rev. Bryol. Lichénol. 1966a. V.34. Р. 929–930.
- Dalby D.H. The growth of plants under reduced light // Stud. Speleol. 1966b. V.1. P. 193–203.
- Dale B. Dinoflagellate resting cysts: ‘‘benthic plankton’’ // Survival strategies of the algae. Ed. by G.A. Fryxell. – Cambridge University Press, Cambridge, UK, 1983. – P. 69–136.
- Dayner D.M., Johansen J.R. Observations on the algal flora of Seneca Cavern, Seneca County, Ohio // Ohio Journal of Science. 1991. V. 91(3). P. 118–121.
- Dobat K. Considerations sur la vegetation cryptogamique des grottes du Jura souabe (sud-ouest de l’allemagne) // Annales de Spéléologie. 1970. V. 25, №4. P. 872–907.
- Eavis A. An up-to-date report of cave exploration around the world // White B. (ed.) Proceedings of 15th International Congress of Speleology, Kerrville, Texas, 2009. – P. 21–25.
- Engel A.S. Karst microbial ecosystems // In: Reitner, J. and Thiel, V. (Eds) Encyclopedia of Geobiology. – Springer Encyclopedia of Earth Sciences Series (EESS, formerly Kluwer Edition), Berlin, Germany, 2011. – P. 521–531.
- Engel A.S. Microbial Diversity of Cave Ecosystems // L.L. Barton et al. (Eds.). Geomicrobiology: Molecular and Environmental Perspective, Springer Science+Business Media B.V., 2010. – P. 219–238.
- Ettl H., Gärtner G. Syllabus der Boden-, Luft- und Flechtenalgen. – Gustav Fischer Verlag, Stuttgart, 1995. – 721 p.
- Falasco E., Ector L., Isaia M., Wetzel C.E., Hoffmann L., Bona F. Diatom flora in subterranean ecosystems: a review // International Journal of Speleology. 2014. V. 43, №3. P. 231–251.
- Falkowski P.G., La Roche J. Acclimation to spectral irradiance in algae // Journal of Phycology. 1991. V. 27. P. 8–14. DOI: https://doi.org/10.1111/j.0022-3646.1991.00008.x
- Forti P. State of the art in the speleological sciences // White B. (Ed.) Proceedings of 15th International Congress of Speleology, Kerrville, Texas, 2009. – P. 26–31.
- Ford D.C. Karst Hydrogeology and Geomorphology // P. Williams (Ed.). Wiley, Chichester, UK, 2007. – 576 p.
- Garbacki N., Ector L., Kostikov I., Hoffmann L. Contribution à l’étude de la flore des grottes de Belgique // Belgian Journal of Botany. 1999. V. 132. P. 43–76.
- Giordano M., Mobili F., Pezzoni V., Hein M.K., Davis J.S. Photosynthesis in the caves of Frasassi (Italy) // Phycologia. 2000. V. 39. P. 384–389. DOI: https://doi.org/10.2216/i0031-8884-39-5-384.1
- Golubić S. Algenvegetation der Felsen: Eine ökologische Algenstudie im dinarischen Karstgebiet // Die Binnengewässer: Band XXIII. E. – Elster H.J., Ohle W. (Eds.) – Schweizerbart'sche Verlagsbuchhandlung, Stuttgart, 1967. – 183 p.
- Golubić S., Friedmann I., Schneider J. The lithobiontic ecological niche, with special reference to microorganisms // J Sediment Petrol. 1981. V.5. P. 475–478. DOI: http://doi.org/10.1306/212F7CB6-2B24-11D7-8648000102C1865D
- Gorbushina A.A., Broughton W.J. Microbiology of the atmosphere rock interface: how biological interactions and physical stresses modulate a sophisticated microbial ecosystem // Annu Rev Microbiol. 2009. V.63. P. 431–450. DOI: https://doi.org/10.1146/annurev.micro.091208.073349
- Grossman A.R., Schaefer M.R., Chiang G.G., Collier J.L. The response of cyanobacteria to environmental conditions: light and nutrients // The Molecular Biology of Cyanobacteria (Ed. By D.A. Bryant). – Kluwer Academic Publishers, Dordrecht, the Netherlands, 1994. – P. 641–675.
- Hernández-Mariné M., Asencio A.D., Canals A., Ariño X., Aboal M., Hoffmann L. Discovery of population of the lime-incrusting genus Loriella (Stigonematales) in Spanish caves // Arch. Hydrobiol. Suppl. Algol. Stud. 1999. V.129, №94. P 121–138. DOI: 10.1127/algol_stud/94/1999/121
- Hernández-Mariné M., Clavero E., Roldán M. Why there is such luxurious growth in the hypogean environments // Algological Studies, 2003. V.109. P. 229–239. DOI: 10.1127/1864-1318/2003/0109-0229
- Hill C., Forti P. Cave minerals of the world – National Speleological Society, Hunstville, Alabama, USA, 1986. – 238 p.
- Hoffmann L. Caves and other low-light environments: aerophitic photoautotrophic microorganisms // Bitton G. (Ed.) Encyclopedia of Environmental Microbiology. – New York: John Wiley & Sons, 2002. – P.835–843.
- Howarth F.G. Ecology of cave arthropods // Annu Rev Entomol. 1983. V. 28. Р. 365–389. DOI: https://doi.org/10.1146/annurev.en.28.010183.002053
- Howarth F.G. The cavernicolous fauna of Hawaiian lava tubes // Pacicific Insects. 1973. V.15(1). P. 139–151.
- Howarth F.G., Moldovan O.T. Where Cave Animals Live // Cave Ecology (Eds. O.T. Moldovan et al.). – Ecological Studies 235, Springer Nature Switzerland AG, 2018. – P. 23–37.
- Ivarsson L.N., Ivarsson M., Lundberg J., Sallstedt T., Rydin C. Epilithic and aerophilic diatoms in the artificial environment of Kungsträdgåden metro station, Stockholm, Sweden // Int. J. Spel. 2013. V.42(3). P. 289–297. DOI: http://doi.org/10.5038/1827-806X.42.3.12
- Jones R.I. Mixotrophy in planktonic protists as a spectrum of nutritional strategies // Marine Microbial Food Webs. 1994. V. 8. P. 87–96.
- Jones R.I. Mixotrophy in planktonic protists: an overview // Freshwater Biology. 2000. V.45. P. 219–226. DOI: https://doi.org/10.1046/j.1365-2427.2000.00672.x
- Kashima N., Irie T., Kinoshita N. Diatom, contributors of coralloid speleothems, from Togawa-Sakaidani-do cave in Miyazaki Prefecture, Central Kyushu, Japan // International Journal of Speleology. 1987. V. 16. P. 95–100. DOI: http://doi.org/10.5038/1827-806X.16.3.3
- Kawecka B. Sessile algal communities in a mountain stream in conditions of light gradation during its flow through a cave (West Tatra, Poland) // Acta Hydrobiologica. 1989. V. 31. P. 35–42.
- Keshari N., Adhikary S.P. Characterization of cyanobacteria isolated from biofilms on stone monuments at Santiniketan, India // Biofouling: The Journal of Bioadhesion and Biofilm Research. 2013. V.29, №5. P. 525–536. DOI: https://doi.org/10.1080/08927014.2013.794224
- Kirk J.T.O. Light and photosynthesis in aquatic ecosystems. – Cambridge, Cambridge University Press, 1983. – 401 p.
- Kirst G.O., Wiencke C. Ecophysiology of polar algae // Journal of Phycology. 1995. V. 31. P. 181–199. DOI: https://doi.org/10.1111/j.0022-3646.1995.00181.x
- Klemenčič A., Vrhovšek D. Algal flora of Krška jama Cave // Acta Mus. Nat. Pragae, Ser. B, Hist. Nat. 2005. V. 61, №1–2. P. 77–80.
- Kol E. Algological investigations in the ice-cave of the Sator mountain. Bot. Kozl. 1957. V.47 P. 43–50.
- Kol E. The microvegetation of a small ice-cave in Hungary // International Journal of Speleology. 1964. V. 1, №1–2. P. 19–24. DOI: http://doi.org/10.5038/1827-806X.1.1.3
- Komáromy Z.P., Padisak J., Rajczy M. Flora in the lamp-lit areas of the cave "Anna-Barlang" near Lillafuered (Hungary) // Ann. Hist. Nat. Mus. Natl. Hung. 1985. V. 77. P. 103–112.
- Koponen T.K. Ceratodon purpureus ja varstasammal Pohlia nutans 176 m syvyydessa Vihannin Kaivoksessa. [Ceratodon purpureus and Pohlia nutans found at a depth of 176 m in the mine at Vihanti, Finland] // Luonnon Tutkija. 1977. V.81. P. 59.
- Krajick K. Cave biologists unearth buried treasure. Science. – 2001. – V. 293. – P. 2378–2381.
- Kubešová S. Bryophyte flora at lamps in public caves in the Moravian Karst (Czech Republic) // Acta. Mus. Morav. Sci. Biol. 2001. V.86, №19. Р.195–202.
- Lakshmi K.S., Jnanendra R., Adhikary S.P. Growth response and protein pro file of two different Scytonema species from cave walls and soil crusts in light and dark // Algol Stud. 2008. V. 127. P.49–60.
- Lamprinou V., Pantazidou A., Papadogiannaki G., Radea C., Economou-Amilli A. Cyanobacteria in Leontari Cave // Fottea. 2009. V.9, №1. P. 155–164. DOI: http://doi.org/10.5507/fot.2009.014
- Lamprinou V., Danielidis D.B., Economou-Amilli A., Pantazidou A. Distribution survey of Cyanobacteria in three Greek caves of Peloponnese // International Journal of Speleology. 2012. V. 41, №2. P. 267–272. DOI: http://doi.org/10.5038/1827-806X.41.2.12
- Lamprinou V., Danielidis D.B., Pantazidou A., Oikonomou A., Economou-Amilli A. The show cave of Diros vs. wild caves of Peloponnese, Greece – distribution patterns of Cyanobacteria // International Journal of Speleology. 2014. V. 43, №3. P. 335–342. DOI: http://doi.org/10.5038/1827-806X.43.3.10
- Lauriol B., Prévost C., Lacelle D. The distribution of diatom flora in ice caves of the northern Yukon Territory, Canada: relationship to air circulation and freezing // International Journal of Speleology. 2006. V. 35, № 2. P. 83–92. DOI: http://doi.org/10.5038/1827-806X.35.2.4
- Lauritzen S.-E. Physiography of the Caves // Cave Ecology. O.T. Moldovan, Ľ. Kováč, S. Halse (Eds.). – Ecological Studies 235, Springer Nature Switzerland AG, 2018. – P. 7–23. DOI: 10.1007/978-3-319-98852-8_2
- Lee N.M., Meisinger D.B., Aubrecht R., Kováčik L., Saiz-Jimenez C., Baskar S., Baskar R., Liebl W., Porter M.L., Engel A.S. Caves and karst environments // Bell E.M. (Ed.) – Life at Extremes: Environments, Organisms and Strategies for Survival. – Wallingford: CAB International, 2012. – P. 320–344.
- Li R., Watanabe M., Watanabe M. Akinete formation in plankton Anabaena spp. (cyanobacteria) by treatment with low temperature // Journal of Phycology. 1997. V. 33. P. 576–584. DOI: https://doi.org/10.1111/j.0022-3646.1997.00576.x
- Luder U.H., Wiencke C., Knoetzel J. Acclimation of photosynthesis and pigments during and after six months of darkness in Palmaria decipiens (Rhodophyta): a study to simulate Antarctic winter sea ice cover // Journal of Phycology. 2002. V. 38. P. 904–913. DOI: https://doi.org/10.1046/j.1529-8817.2002.t01-1-01071.x
- Lund J.W.G. Observations on soil algae. I. The ecology, size and taxonomy of British soil diatoms // New Phytologist. 1946. V. 45. P. 56–110. DOI: https://doi.org/10.1111/j.1469-8137.1946.tb05047.x
- Macedo M.F., Miller A.Z., Dionísio A., Saiz-Jimenez C. Biodiversity of cyanobacteria and green algae on monuments in the Mediterranean Basin: an overview // Microbiology. 2009. V. 155. Р.3476–3490. DOI: https://doi.org/10.1099/mic.0.032508-0
- MacIntyre H.L., Kana T.M., Anning T., Geider R.J. Photoacclimation of photosynthesis irradiance response curves and photosynthetic pigments in microalgae and cyanobacteria // Journal of Phycology. 2002. V. 38. P. 17–38. DOI: https://doi.org/10.1046/j.1529-8817.2002.00094.x
- Mandić M., Mihevc A., Leis A., Krajcar Bronić I. Concentration and stable carbon isotopic composition of CO2 in cave air of Postojnska jama, Slovenia // International Journal of Speleology. 2013. V. 42, №3. P. 279–287. DOI: http://doi.org/10.5038/1827-806X.42.3.11
- Martinez A., Asencio A.D. Distribution of Cyanobacteria at the Gelada Cave (Spain) by physical parameters // Journal of Cave and Karst Studies. 2010. V. 72, №. 1. P. 11–20. DOI: 10.4311/jcks2009lsc0082
- Martinčič A., Vrhovšek D., Batič F. Flora v jamah z umetno osvetlitvijo // Biološki Vestnik. 1981. V. 29, № 2. P.27–56.
- Mattey D.P., Atkinson T.C., Barker J.A., Fisher R., Latin J.-P., Durell R., Ainsworth M. Carbon dioxide, ground air and carbon cycling in Gibraltar karst // Geochimica et Cosmochimica Acta. 2016. V. 184. Р. 88–113. DOI: https://doi.org/10.1016/j.gca.2016.01.041
- McQuoid M.R., Hobson L.A. Review: diatom resting stages // Journal of Phycology. 1996. V. 32. P. 889–902. DOI: https://doi.org/10.1111/j.0022-3646.1996.00889.x
- Miskiewicz E., Ivanov A.G., Williams J.P., Khan M.U., Falk S., Huner N.P.A. Photosynthetic acclimation of the filamentous cyanobacterium, Plectonema boryanum UTEX 485 to temperature and light // Plant Cell Physiology. 2000. V.41, №6. P. 767–775. DOI: https://doi.org/10.1093/pcp/41.6.767
- Mulec J., Kosi G. Algae in the aerophytic habitat of Račiške ponikve cave (Slovenia) // Natura Sloveniae. 2008. V.10, №1. P. 39–49. DOI: https://doi.org/10.14720/ns.10.1.39-49
- Mulec J., Kosi G. Lampenflora algae and methods of growth control // Journal of Cave and Karst Studies. 2009. V.71, №2. P 109–115.
- Mulec J., Kosi G., Vrhovsˇek D. Characterization of cave aerophytic algae communities and effects of irradiance levels on production of pigments // Journal of Cave and Karst Studies. 2008. V. 70, №. 1. P. 3–12.
- Mulec J., Kubešová S. Diversity of bryophytes in show caves in Slovenia and relation to light intensities // Acta Carsologica. 2010. V.39, №3. P.587–596. DOI: https://doi.org/10.3986/ac.v39i3.86
- Murphy A.M., Cowles T.J. Effects of darkness on multiexcitation in vivo fluorescence and survival in a marine diatom // Limnology & Oceanography. 1997. V.42, №6. P. 1444–1453. DOI: https://doi.org/10.4319/lo.1997.42.6.1444
- Northup D.E., Lavoie K.H. Geomicrobiology of Caves: A Review // Geomicrobiology Journal. 2001. V.18, №3. P. 199–222. DOI: https://doi.org/10.1080/01490450152467750
- Opsahl S.P., Chanton J.P. Isotopic evidence for methane-based chemosynthesis in the Upper Floridan aquifer food web // Oecologia. 2006. V.150, №1. P. 89–96. JSTOR. DOI: 10.1007/s00442-006-0492-2
- Palik P. A barlangok algavilágáról (Study into the algal flora of caves) // Hidrológiai Közlöny. 1960. V. 40. P. 417–422.
- Palmer A.N. Origin and morphology of limestone caves // Geological Society of America Bulletin. 1991. V. 103. Р.1–21.
- Patrick R. Factors effecting the distribution of diatoms // The Botanical Review. 1948. V. 14. P. 473–524.
- Pattanaik B., Schumann R., Karsten U. Effects of ultraviolet radiation on cyanobacteria and their protective mechanisms // Seckbach J. (Ed.) Algae and cyanobacteria in extreme environments. – Springer, Dordrecht, 2007. – P. 29–45. DOI: https://doi.org/10.1007/978-1-4020-6112-7_2
- Pentecost A., Zhaohui Z. The distribution of plants in Scoska Cave, North Yorkshire, and their relationship to light intensity // International Journal of Speleology. 2001. V.30, №1. P. 27–37.
- Petersen J.B. The aërial Algae of Iceland // Rosenvinge L.K. & Warming E. (Eds.). The Botany of Iceland. J. Frimodt, Copenhagen, 1928. – V. 2, №8. – P. 325–447.
- Pfendler S., Karimi B., Maron P.-A., Ciadamidaro L., Valot B., Bousta F., Alaoui-Sosse L., Alaoui-Sosse B., Aleya L. Biofilm biodiversity in French and Swiss show caves using the metabarcoding approach: First data // Science of the Total Environment. 2018. V. 615. P. 1207–1217. DOI: https://doi.org/10.1016/j.scitotenv.2017.10.054
- Popović S., Simić G.S., Stupar M., Unković N., Jovanović J., Grbić M.L. Cyanobacteria, algae and microfungi present in biofilm from Božana Cave (Serbia) // International Journal of Speleology. 2015. V. 44(2). P. 141–149. DOI: http://doi.org/10.5038/1827-806X.44.2.4
- Porter M.L., Engel A.S., Kinkle B., Kane T.C. Productivity-diversity relationships from chemolithoautotrophically based sulfidic karst systems // Int J Speleol. 2009. V. 38. P. 27–40. DOI: http://doi.org/10.5038/1827-806X.38.1.4
- Poulíčková A., Hašler P. Aerophytic diatoms from caves in central Moravia (Czech Republic) // Preslia. 2007. V.79. P.185–204.
- Poulson T.L., White W.B. The Cave Environment // Science. 1969. V.165, №3897. Р.971–981. DOI: 10.1126/science.165.3897.971
- Puglisi M., Privitera M., Minissale P., Costa R. Diversity and ecology of the bryophytes in the cave environment: a study on the volcanic and karstic caves of Sicily // Plant Biosystems–An International Journal Dealing with all Aspects of Plant Biology. 2019. V.153, №1. P. 134–146. DOI: https://doi.org/10.1080/11263504.2018.1478903
- Raboy B., Padan E. Active transport of glucose and alpha-methyglucoside in cyanobacterium Plectonema boryanum // Journal of Biological Chemistry. 1978. V.253(9). P. 3287–3291.
- Racovitza E.G. Éssai sur les problèmes biospéleologiques // Arch. Zool. Exp. Générale. 1907. V.6. P. 371–488.
- Reinoso F.J., Viera Benitez M.C., Rodriguez O.J. Precisions on the ecology and chorology of Schistostega pennata (Hedw.) Webb & Mohr. in the Iberian Peninsula // Lazaroa. 1994. V.14. P.13–19.
- Rajczy M. The flora of Hungarian caves // Karszt és Barlang. (Spec. issue). Budapest. 1989. Р. 69–72.
- Rengefors K., Anderson D.M. Environmental and endogenous regulation of cyst germination in two fresh-water dinoflagellates // Journal of Phycology. 1998. V. 34. P. 568–577. DOI: https://doi.org/10.1046/j.1529-8817.1998.340568.x
- Roldán M., Clavero E., Canals T., Gómez-Bolea A., Ariño X., Hernández-Mariné M. Distribution of phototrophic biofilms in cavities (Garraf, Spain) // Nova Hedwigia. 2004. V.78. P. 329–351. DOI: 10.1127/0029-5035/2004/0078-0329
- Roldán M., Hernández-Mariné M. Exploring the secrets of the three-dimensional architecture of phototrophic biofilms in caves // International Journal of Speleology. 2009. V.38, №1. P. 41–53. DOI: http://doi.org/10.5038/1827-806X.38.1.5
- Rother J.A., Fay P. Sporulation and the development of planktonic blue-green algae in two Salopian meres // Proceedings of the Royal Society of London, Series B: Biological Science. 1977. V.196 (1124). P. 317–332. DOI: https://doi.org/10.1098/rspb.1977.0043
- Sarbu S.M., Kane T.C., Kinkle B.K. A chemoautotrophically based cave ecosystem // Science. 1996. V.272 (5270). Р. 1953–1955. DOI: 10.1126/science.272.5270.1953
- Selvi B., Altuner Z. Algae of Ballıca Cave (Tokat-Turkey) // International Journal of Natural and Engineering Sciences. 2007. V.1, №3. P.99–103.
- Sicko-Goad L., Stoermer E.F., Kociolek J.P. Diatom resting cell rejuvenation and formation: time course, species records and distribution // Journal of Plankton Research. 1989. V.11(2). P. 375–389. DOI: https://doi.org/10.1093/plankt/11.2.375
- Šmarda J. Flóra kolem jeskynních reflektorů // Absolon K. Moravský kras. II. – Praha: Academia, 1970. – P. 304–305. (In Czech)
- Smith J.K.P., Hughes A.D., McEvoy L., Day J.D. Tailoring of the biochemical profiles of microalgae by employing mixotrophic cultivation // Bioresource Technology Reports. 2020. V.9. ID 100321. DOI: https://doi.org/10.1016/j.biteb.2019.100321
- Smith T., Olson R. A taxonomic survey of lamp flora (Algae and Cyanobacteria) in electrically lit passages within Mammoth Cave National Park, Kentucky // International Journal of Speleology. 2007. V.36, №2. P.105–114. DOI: http://doi.org/10.5038/1827-806X.36.2.6
- Souffreau C., Vanormelingen P., Verleyen E., Sabbe K., Vyverman W. Tolerance of benthic diatoms from temperate aquatic and terrestrial habitats to experimental desiccation and temperature stress // Phycologia. 2010. V.49(4). P. 309–324. DOI: https://doi.org/10.2216/09-30.1
- St. Clair L.L., Rushforth S.R., Allen J.V. Diatoms of Oregon Caves National Monument, Oregon // Great Basin Naturalist. 1981. V.41 (3). P. 317–332.
- St. Clair L.L., Rushforth S.R. The diatoms of Timpanogos Cave National Monument, Utah // American Journal of Botany. 1976. V.63(1). P. 49–59. DOI: https://doi.org/10.1002/j.1537-2197.1976.tb11784.x
- Stal L.J. Cyanobacterial mats and stromatolites // Whitton B.A. & Potts M. (Eds.) – The Ecology of the Cyanobacteria: Their Diversity in Space and Time. – Dordrecht, Kluwer Academic Publishers, 2000. – P.61–120.
- Thatcher E.P. Bryophytes of an artificially illuminated cave // Bryologist. 1949. V.52 (4). P. 212–214.
- Tilzer M.M., Paerl H.W., Goldman C.R. Sustained viability of aphotic phytoplankton in Lake Tahoe (California-Nevada) // Limnology & Oceanography. 1977. V.22. P. 84–91.
- Uher B., Kováčik L. Epilithic cyanobacteria of subaerial habitats in National Park Slovak Paradise (1998–2000) // Bull. Slov. Bot. Spoločn., Bratislava. 2002. V.24. P. 25–29.
- Whitton B.A., Potts M. The ecology of cyanobacteria: their diversity in time and space. – Dordrecht, London, Boston: Kluwer Academic Publishers, 2000. – 669 p.
- Yentsch C.S., Reichert C.A. The effects of prolonged darkness on photosynthesis, respiration, and chlorophyll in the marine flagellate, Dunaliella euchlora // Limnology & Oceanography. 1963. V.8 (3). P. 338–342. DOI: https://doi.org/10.4319/lo.1963.8.3.0338
- Young E., Beardall J. Transient perturbations in chlorophyll a fluorescence elicited by nitrogen re-supply to nitrogen-stressed microalgae: distinct responses to NO3 versus NH4 // Journal of Phycology. 2003. V.39. P. 332–342.
- Zammit G., Billi D., Albertano P. The subaerophytic cyanobacterium Oculatella subterranea (Oscillatoriales, Cyanophyceae) gen. et sp. nov: a cytomorphological and molecular description // Euro J Phycol. 2012. V.47(4). P. 314–354. DOI: https://doi.org/10.1080/09670262.2012.717106
- Zammit G., Billi D., Shubert E., Kaštovský J., Albertano P. The biodiversity of subaerophytic phototrophic biofilms from Maltese hypogeal // Fottea. 2011. V.11 (1). P. 187–201. DOI: 10.5507/fot.2011.018
Статья поступила в редакцию 19.03.2024
Статья поступила после доработки 01.11.2024
Статья принята к публикации 18.12.2024
Об авторе
Попкова Анна Владимировна – Popkova Anna V.
кандидат биологических наук
зам. директора по международной деятельности Института экологии Российского университета дружбы народов им. Патриса Лумумбы (РУДН), г. Москва, Россия (RUDN University, Moscow, Russia); РИНЦ SPIN-код: 3431-6569, AuthorID: 876076
popkova_av@pfur.ru
Корреспондентский адрес: Россия, 117198, г. Москва, ул. Миклухо-Маклая, 6, РУДН; тел. (495)952-89-01.
ССЫЛКА НА СТАТЬЮ:
Попкова А. В. Экологические особенности и биоразнообразие фототрофов карстовых пещер // Вопросы современной альгологии. 2024. № 2–3 (35–36). С. 84–109. URL: http://algology.ru/2102
DOI - https://doi.org/10.33624/2311-0147-2024-2-3(35-36)-84-109; EDN – GANSCS
Уважаемые коллеги! Если Вы хотите получить весию стратьи в формате PDF, пожалуйста, напишите в редакцию, и мы ее вам с удовольствием пришлем бесплатно.
Адрес - info@algology.ru
При перепечатке ссылка на сайт обязательна
.
Ecological features and biodiversity of phototrophic organisms
in karst caves
Anna V. Popkova
RUDN University (Moscow, Russia)
Karst areas (caves) occupy 15–20% of the Earth's land surface, making them incredibly interesting and important for research. Despite this, underground cavities are among the least studied habitats on Earth. This review presents data on the specific features of underground habitats, as well as the ecological characteristics and biodiversity of phototrophs in their ecosystems. Various groups of phototrophs inhabiting caves are described. The mechanisms by which phototrophic organisms adapt to underground habitats are discussed, including the characteristics of photosynthesis. Issues related to the influence of environmental factors such as temperature, humidity, and photon flux levels on the distribution of organisms in caves are considered. Particular attention is paid to studies of entrance zones and their biota. It is shown that the isolation of cave entrance areas allows them to be considered ecotones with a unique set of environmental parameters. It is suggested that cave entrance zones may function as refugia, harbouring unique species of rare and endangered organisms. Attention is paid to the mixotrophic status of algae and cyanobacteria living in low light or darkness. It is noted that cave landscapes are particularly important due to significant anthropogenic landscape changes and the accompanying habitat loss.
Key words: karst caves; cave classification; karst cave biota; ecological factors of karst caves; phototrophs of karst caves; adaptation of phototrophs to darkness
References
- Abdullin Sh.R. Biodiversity of cyanobacteria and algae of the Askin cave (Southern Urals). Vestnik OGU. 2009. №6. P. 9–10. (In Russ.)
- Abdullin Sh.R. Trophic structure diversity of cave ecosystems. Uspekhi sovremennoj biologii. 2014. V. 134, №2. P. 192–204. (In Russ.)
- Abdullin Sh.R. Regularities of diversity formation and taxonomy of cyanobacterial-algal coenoses in caves of russia and some neighboring states: Dr.Sci. Thesis. Ufa, BGU, 2015. 440 p. (In Russ.)
- Abdullin Sh.R., Bagmet V.B. Myxotrophy of cyanobacteriae and algae inhabiting caves. Zhurnal obshchej biologii. 2016. Т. 77, № 1. P. 54–62. (In Russ.)
- Abdullin Sh.R., Sharipova М.Yu. Algal flora of Shulgan-Tash (Kapova) Cave in different years. Vestnik Bashkirskogo universiteta. 2005. №3. P. 49–50. (In Russ.)
- Aboal M., Asencio A.D., Prefasi M. Studies on cave cyanophytes from southeastern Spain: Scytonema julianum (Meneghini ex Franck) Richter. Algological Studies/Arch Hydrobiol Suppl. 1994. V.75. P. 31–36. DOI: https://doi.org/10.1127/algol_stud/75/1995/31
- Adhikary S.P. Survival in darkness and heterotrophic growth of epilithic cyanobacteria from temples of India. Algological Studies/Arch Hydrobiol Suppl. 2002. V.105. P. 141–155. DOI: https://doi.org/10.1127/algol_stud/105/2002/141
- Albertano P. Cyanobacterial Biofilms in Monuments and Caves. In: B.A. Whitton (ed.), Ecology of Cyanobacteria II: Their Diversity in Space and Time. Springer Dordrecht, Springer Science+Business Media B.V., 2012. P. 317–345.
- Albertano P. Epilithic algal communities in hypogean environments. Giornale Botanico Italiano. 1993. V.127. P. 386–392. DOI: http://doi.org/10.1080/11263509309431020
- Albertano P., Bruno L., Bellezza S. New strategies for the monitoring and control of cyanobacterial films on valuable lithic faces. Plant Biosystems. 2005. V.139. P. 311–322. DOI: http://doi.org/10.1080/11263500500342256
- Albertano P., Urzí C. Structural interactions among epilithic Cyanobacteria and heterotrophic Microorganisms in Roman Hypogea. Microbial ecology. 1999. V.38. P. 244–252. DOI: http://doi.org/10.1007/s002489900174
- Albertano P., Barsanti L., Passarelli V., Gualtieri P. A complex photoreceptive structure in the cyanobacterium Leptolyngbya sp. Micron. 2000. V.31. P. 27–34. DOI: https://doi.org/10.1016/S0968-4328(99)00063-3
- Allaguvatova R.Z., Nikulin A.Yu., Bagmet V.B., Abdullin Sh.R. Cyanobacteria and algae biodiversity of grounds and soils from south Kamchatka volcanoes. Vestnik of the FEB RAS. 2022. №5. P. 75–87. DOI: http://doi.org/10.37102/0869-7698_2022_225_05_6 (In Russ.)
- Altieri A., Pietrini A.M., Ricci S. Un’associazione di alghe e muschi in un sito archeologico ipogeo. Giornale Botanico Italiano. 1993. V.127. P. 611.
- Ariño X., Hernández-Mariné M., Saiz-Jimenez C. Colonization of Roman tombs by calcifying cyanobacteria. Phycologia. 1997. V.36. P. 366–373.
- Asencio A.D., Aboal M. Cell inclusions in the chasmoendolithic Cyanophytes from cave-like environments in Murcia (SE Spain). Algological Studies/Arch Hydrobiol Suppl. 2004. V. 113. P. 117–127. DOI: https://doi.org/10.1127/1864-1318/2004/0113-0117
- Bahls L.L. Diatoms of Lewis and Clark Caverns // Proceedings of the Montana Academy of Sciences. 1981. V.40. P.11–18.
- Baković N., Pipan T., Baković R., Ozimec R., Rubinić J., Matoničkin Kepčija R. Algae and cyanobacteria in the aphotic habitats of Veternica Cave (Medvednica Mt., Croatia) and selected caves of the Dinaric karst (Southeast Europe). International Journal of Speleology. 2022. V.51(3). P. 193–203. DOI: https://doi.org/10.5038/1827-806X.51.3.2422
- Balskus E.P., Walsh C.T. Investigating the initial steps in the biosynthesis of cyanobacterial sunscreen scytonemin. Journal of the Chemical American Society. 2008. V.130, №46. P. 15260–15261. DOI: https://doi.org/10.1021/ja807192u
- Bellezza S., Albertano P., de Philippis R., Paradossi G. Exopolysaccharides of two cyanobacterial strains from Roman hypogeal. Geomicrobiology Journal. 2006. V.23. P. 301–310. DOI: https://doi.org/10.1080/01490450600761904
- Bellezza S., Paradossi G., De Philippis R., Albertano P. Leptolyngbya strains from Roman hypogea: cytochemical and physico-chemical characterisation of exopolysaccharides. Journal of Applied Phycology. 2003. V.15. P. 193–200. DOI: https://doi.org/10.1023/A:1023811311686
- Bock W. Diatomeen extrem trockener Standorte. Nova Hedwigia. 1963. V. 5. P. 99–254.
- Bonacci O., Pipan T., Culver D.C. A framework for karst ecohydrology. Environ Geol. 2009. V.56. P. 891–900. DOI: https://doi.org/10.1007/s00254-008-1189-0
- Buczkó K. Diadesmis brekkaensoides (W. Bock) Moser, Lang.e-Bertalot et Metzeltin: a new aerophytic diatom for the Hungarian flora. Studia Botanica Hungarica. 2003. V.34. P. 5–10.
- Buczkó K., Rajczy M. Contributions to the flora of the Hungarian caves II. Flora of the three caves near Beremend, Hungary. Studia Botanica Hungarica. (Antea: Fragmenta Botanica). 1989. V.21. P. 13–25.
- Bunt J.S., Lee C.C. Data on the composition and dark survival of four sea-ice microalgae // Limnology & Oceanography. 1972. V.17. P. 458–462.
- Carter J.R. Diatoms from the Devil’s Hole Cave Fife, Scotland. Nova Hedwigia. 1971. V.21. P. 657–681.
- Cennamo P., Marzano C., Ciniglia C., Pinto G., Cappelletti P., Caputo P., Pollio A. A survey of the algal flora of anthropogenic caves of Campi Flegrei (Naples, Italy) archeological district. Journal of Cave and Karst Studies. 2012. V.74, №3. P. 243–250. DOI: 10.4311/2011JCKS0194
- Chapman A.D., Pfiester L.A. The effects of temperature, irradiance, and nitrogen on the encystment and growth of the freshwater dinoflagellates Peridinium cinctum and Peridinium willei in culture (Dinophyceae). Journal of Phycology. 1995. V. 31. P. 355–359.
- Chen G.Q., Chen F. Growing phototrophic cells without light. Biotechnology Letters. 2006. V. 28. P. 607–616. DOI: https://doi.org/10.1007/s10529-006-0025-4
- Chen Y., Wu L., Boden R., Hillebrand A., Kumaresan D., Moussard H., Baciu M., Lu Y., Murrell J.C. Life without light: microbial diversity and evidence of sulfur- and ammonium-based chemolithotrophy in Movile Cave. ISME J. 2009. V.3. P. 1093–1104. DOI: https://doi.org/10.1038/ismej.2009.57
- Chodat R. Étude critique et expérimentale sur le polymorphisme des algues. – Genève: Georg & Cie, 1909. – 165 p.
- Claus G. Algae and their mode of life in the Baradla cave at Aggtelek. Act. Bot. Acad. Sc. Hungar. 1955. V.2, №1–2. P. 1–26.
- Conard H.S. Cave mosses. Bryologist. 1932. 13 p.
- Couté A., Chauveau O. Algae. In: Juberthie C. & Decu V. (Eds.) Encyclopaedia Biospeologica 1. Société de Biospéléologie. Moulis–Bucarest, 1994. P. 371–380.
- Couté A. Ultrastructure d'une cyanophycée aérienne calcifiée cavernicole: Geitleria calcarea Friedmann. Hydrobiologia. 1982. V.97. P. 255–274. DOI: https://doi.org/10.1007/BF00007113
- Cowan B.D., Osborne M.C., Banner J.L. Temporal variability of cave-air CO2 in central Texas. Journal of Cave and Karst Studies. 2013. V.75, №1. P. 38–50. DOI: 10.4311/2011ES0246
- Cox G., James J.M., Leggett K.E.A., Osborne R.A.L. Cyanobacterially deposited speleothems: Subaerial stromatolites // Geomicrobiology J. 1989. V.7. Р. 245–252.
- Culver D.C., Pipan T. The biology of caves and other subterranean habitats. Oxford University Press, 2009. P. 1−273.
- Czerwik-Marcinkowska J. Observations on aerophytic cyanobacteria and algae from ten caves in the Ojców national park. Acta Agrobotanica. 2013. V.66, №1. P.39–52. DOI: https://doi.org/10.5586/aa.2013.005
- Czerwik-Marcinkowska J., Mrozińska T. Algae and cyanobacteria in caves of the Polish Jura. Polish Botanical Journal. 2011. V.56, №2. P. 203–243. (In Polish)
- Czerwik-Marcinkowska J., Mrozińska T. Epilithic algae from caves of the Krakowsko-Czestochowska upland (Southern Poland). Acta Societatis Botanicorum Poloniae. 2009. V.78, №4. P. 301–309. DOI: https://doi.org/10.5586/asbp.2009.040
- Dalby D.H. The growth of Eucladium verticillatum in a poorly illuminated cave. Rev. Bryol. Lichénol. 1966a. V.34. Р. 929–930.
- Dalby D.H. The growth of plants under reduced light. Stud. Speleol. 1966 b. V.1. P. 193–203.
- Dale B. Dinoflagellate resting cysts: ‘‘benthic plankton’’. In: Survival strategies of the algae. Ed. by G.A. Fryxell. Cambridge University Press, Cambridge, UK, 1983. P. 69–136.
- Dayner D.M., Johansen J.R. Observations on the algal flora of Seneca Cavern, Seneca County, Ohio. Ohio Journal of Science. 1991. V. 91. P. 118–121.
- Dobat K. Considerations sur la vegetation cryptogamique des grottes du Jura souabe (sud-ouest de l’allemagne). Annales de Spéléologie. 1970. V. 25, №4. P. 872–907.
- Eavis A. An up-to-date report of cave exploration around the world. In: White B. (Ed.) Proceedings of 15th International Congress of Speleology, Kerrville, Texas, 2009. P. 21–25.
- Engel A.S. Karst microbial ecosystems. In: Reitner, J. and Thiel, V. (Eds) Encyclopedia of Geobiology. Springer Encyclopedia of Earth Sciences Series (EESS, formerly Kluwer Edition), Berlin, Germany, 2011. P. 521–531.
- Engel A.S. Microbial Diversity of Cave Ecosystems In: L.L. Barton et al. (eds.). Geomicrobiology: Molecular and Environmental Perspective, Springer Science+Business Media B.V., 2010. P. 219–238.
- Ettl H., Gärtner G. Syllabus der Boden-, Luft- und Flechtenalgen. – Gustav Fischer Verlag, Stuttgart, 1995. – 721 p.
- Falasco E., Ector L., Isaia M., Wetzel C.E., Hoffmann L., Bona F. Diatom flora in subterranean ecosystems: a review. International Journal of Speleology. 2014. V. 43, №3. P. 231–251.
- Falkowski P.G., La Roche J. Acclimation to spectral irradiance in algae. Journal of Phycology. 1991. V. 27. P. 8–14. DOI: https://doi.org/10.1111/j.0022-3646.1991.00008.x
- Forti P. State of the art in the speleological sciences. In: White B. (Ed.) Proceedings of 15th International Congress of Speleology, Kerrville, Texas, 2009. P. 26–31.
- Ford D.C. Karst Hydrogeology and Geomorphology. In: P. Williams. Wiley, Chichester, UK, 2007. 576 p.
- Garbacki N., Ector L., Kostikov I., Hoffmann L. Contribution à l’étude de la flore des grottes de Belgique // Belgian Journal of Botany. 1999. V. 132. P. 43–76.
- Giordano M., Mobili F., Pezzoni V., Hein M.K., Davis J.S. Photosynthesis in the caves of Frasassi (Italy). Phycologia. 2000. V. 39. P. 384–389. DOI: https://doi.org/10.2216/i0031-8884-39-5-384.1
- Golubić S. Algenvegetation der Felsen: Eine ökologische Algenstudie im dinarischen Karstgebiet. In: Elster H.J., Ohle W. (Eds.), Die Binnengewässer: Band XXIII. E. Schweizerbart'sche Verlagsbuchhandlung, Stuttgart, 1967. 183 p.
- Golubić S., Friedmann I., Schneider J. The lithobiontic ecological niche, with special reference to microorganisms. J Sediment Petrol. 1981. V.5. P. 475–478. DOI: http://doi.org/10.1306/212F7CB6-2B24-11D7-8648000102C1865D
- Gorbunova S.Yu., Zhondareva Ya.D Mixotrophic food as an example of environmentally friendly technology for the cultivation of cyanobacteria Arthrospira (Spirulina) platensis (Nordst) Geitler. Voprosy sovremennoi algologii (Issues of modern algology). 2017. № 2 (14). URL: http://algology.ru/1176 (date: 10.02.2024) (In Russ.)
- Gorbushina A.A., Broughton W.J. Microbiology of the atmosphere rock interface: how biological interactions and physical stresses modulate a sophisticated microbial ecosystem. Annu Rev Microbiol. 2009. V.63. P. 431–450. DOI: https://doi.org/10.1146/annurev.micro.091208.073349
- Grossman A.R., Schaefer M.R., Chiang G.G., Collier J.L. The response of cyanobacteria to environmental conditions: light and nutrients // In: The Molecular Biology of Cyanobacteria (Ed. By D.A. Bryant). Kluwer Academic Publishers, Dordrecht, the Netherlands, 1994. P. 641–675.
- Hernández-Mariné M., Asencio A.D., Canals A., Ariño X., Aboal M., Hoffmann L. Discovery of population of the lime–incrusting genus Loriella (Stigonematales) in Spanish caves. Arch. Hydrobiol. Suppl. Algol. Stud. 1999. V.129, №94. P 121–138. DOI: 10.1127/algol_stud/94/1999/121
- Hernández-Mariné M., Clavero E., Roldán M. Why there is such luxurious growth in the hypogean environments. Algological Studies. 2003. V. 109. P. 229–239. DOI: 10.1127/1864-1318/2003/0109-0229
- Hill C., Forti P. Cave minerals of the world. National Speleological Society, Hunstville, Alabama, USA, 1986. 238 p.
- Hoffmann L. Caves and other low-light environments: aerophitic photoautotrophic microorganisms. In: Bitton G. (Ed.) Encyclopedia of Environmental Microbiology. John Wiley & Sons, New York, 2002. P.835–843.
- Howarth F.G. Ecology of cave arthropods. Annu Rev Entomol. 1983. V. 28. Р. 365–389. DOI: https://doi.org/10.1146/annurev.en.28.010183.002053
- Howarth F.G. The cavernicolous fauna of Hawaiian lava tubes. Pacicific Insects. 1973. V.15(1). P. 139–151.
- Howarth F.G., Moldovan O.T. Where Cave Animals Live. In: Cave Ecology (Eds. O.T. Moldovan et al.). Ecological Studies 235, Springer Nature Switzerland AG, 2018. P. 23–37.
- Ivarsson L.N., Ivarsson M., Lundberg J., Sallstedt T., Rydin C. Epilithic and aerophilic diatoms in the artificial environment of Kungsträdgåden metro station, Stockholm, Sweden. Int. J. Spel. 2013. V.42(3). P. 289–297. DOI: http://doi.org/10.5038/1827-806X.42.3.12
- Jones R.I. Mixotrophy in planktonic protists as a spectrum of nutritional strategies. Marine Microbial Food Webs. 1994. V. 8. P. 87–96.
- Jones R.I. Mixotrophy in planktonic protists: an overview. Freshwater Biology. 2000. V.45. P. 219–226. DOI: https://doi.org/10.1046/j.1365-2427.2000.00672.x
- Kashima N., Irie T., Kinoshita N. Diatom, contributors of coralloid speleothems, from Togawa-Sakaidani-do cave in Miyazaki Prefecture, Central Kyushu, Japan. International Journal of Speleology. 1987. V. 16. P. 95–100. DOI: http://doi.org/10.5038/1827-806X.16.3.3
- Kawecka B. Sessile algal communities in a mountain stream in conditions of light gradation during its flow through a cave (West Tatra, Poland). Acta Hydrobiologica. 1989. V. 31. P. 35–42.
- Keshari N., Adhikary S.P. Characterization of cyanobacteria isolated from biofilms on stone monuments at Santiniketan, India. Biofouling: The Journal of Bioadhesion and Biofilm Research. 2013. V.29, №5. P. 525–536. DOI: https://doi.org/10.1080/08927014.2013.794224
- Kirk J.T.O. Light and photosynthesis in aquatic ecosystems. Cambridge, Cambridge University Press, 1983. 401 p.
- Kirst G.O., Wiencke C. Ecophysiology of polar algae. Journal of Phycology. 1995. V.31. P. 181–199. DOI: https://doi.org/10.1111/j.0022-3646.1995.00181.x
- Klemenčič A., Vrhovšek D. Algal flora of Krška jama Cave. In: Acta Mus. Nat. Pragae, Ser. B, Hist. Nat. 2005. V. 61, №1–2. P. 77–80.
- Kol E. Algological investigations in the ice-cave of the Sator mountain. Bot. Kozl. 1957. V.47 P. 43–50.
- Kol E. The microvegetation of a small ice-cave in Hungary. International Journal of Speleology. 1964. V.1, №1–2. P. 19–24. DOI: http://doi.org/10.5038/1827-806X.1.1.3
- Komáromy Z.P., Padisak J., Rajczy M. Flora in the lamp-lit areas of the cave "Anna-Barlang" near Lillafuered (Hungary) // Ann. Hist. Nat. Mus. Natl. Hung. 1985. V. 77. P. 103–112.
- Koponen T.K. Ceratodon purpureus ja varstasammal Pohlia nutans 176 m syvyydessa Vihannin Kaivoksessa. [Ceratodon purpureus and Pohlia nutans found at a depth of 176 m in the mine at Vihanti, Finland]. Luonnon Tutkija. 1977. V.81. P. 59.
- Kozlova E.V. Structural and functional characteristics of the communities in the entrance zones of Montenegro's karst caves: PhD Thesis. Moscow, 2021. 221p. (In Russ.)
- Krajick K. Cave biologists unearth buried treasure. Science. – 2001. – V. 293. – P. 2378–2381.
- Kubešová S. Bryophyte flora at lamps in public caves in the Moravian Karst (Czech Republic). Acta. Mus. Morav. Sci. Biol. 2001. V.86, №19. Р.195–202.
- Lakshmi K.S., Jnanendra R., Adhikary S.P. Growth response and protein pro file of two different Scytonema species from cave walls and soil crusts in light and dark. Algol Stud. 2008. V. 127. P.49–60.
- Lamprinou V., Pantazidou A., Papadogiannaki G., Radea C., Economou-Amilli A. Cyanobacteria in Leontari Cave. Fottea. 2009. V. 9, №1. P. 155–164. DOI: http://doi.org/10.5507/fot.2009.014
- Lamprinou V., Danielidis D.B., Economou-Amilli A., Pantazidou A. Distribution survey of Cyanobacteria in three Greek caves of Peloponnese. International Journal of Speleology. 2012. V. 41, №2. P. 267–272. DOI: http://doi.org/10.5038/1827-806X.41.2.12
- Lamprinou V., Danielidis D.B., Pantazidou A., Oikonomou A., Economou-Amilli A. The show cave of Diros vs. wild caves of Peloponnese, Greece – distribution patterns of Cyanobacteria. International Journal of Speleology. 2014. V. 43, №3. P. 335–342. http://doi.org/10.5038/1827-806X.43.3.10
- Lauriol B., Prévost C., Lacelle D. The distribution of diatom flora in ice caves of the northern Yukon Territory, Canada: relationship to air circulation and freezing. International Journal of Speleology. 2006. V. 35, № 2. P. 83–92. DOI: http://doi.org/10.5038/1827-806X.35.2.4
- Lauritzen S.-E. Physiography of the Caves. In: Cave Ecology. Eds. by O.T. Moldovan, Ľ. Kováč, S. Halse. Ecological Studies 235, Springer Nature Switzerland AG, 2018. P. 7–23. DOI: https://doi.org/10.1007/978-3-319-98852-8_2
- Lee N.M., Meisinger D.B., Aubrecht R., Kováčik L., Saiz-Jimenez C., Baskar S., Baskar R., Liebl W., Porter M.L., Engel A.S. Caves and karst environments. In: Bell E.M. (Ed.) Life at Extremes: Environments, Organisms and Strategies for Survival. Wallingford: CAB International, 2012. P. 320–344.
- Li R., Watanabe M., Watanabe M. Akinete formation in plankton Anabaena spp. (cyanobacteria) by treatment with low temperature. Journal of Phycology. 1997. V.33. P. 576–584. DOI: https://doi.org/10.1111/j.0022-3646.1997.00576.x
- Luder U.H., Wiencke C., Knoetzel J. Acclimation of photosynthesis and pigments during and after six months of darkness in Palmaria decipiens (Rhodophyta): a study to simulate Antarctic winter sea ice cover. Journal of Phycology. 2002. V.38. P. 904–913. DOI: https://doi.org/10.1046/j.1529-8817.2002.t01-1-01071.x
- Lund J.W.G. Observations on soil algae. I. The ecology, size and taxonomy of British soil diatoms. New Phytologist. 1946. V.45. P. 56–110. DOI: https://doi.org/10.1111/j.1469-8137.1946.tb05047.x
- Macedo M.F., Miller A.Z., Dionísio A., Saiz-Jimenez C. Biodiversity of cyanobacteria and green algae on monuments in the Mediterranean Basin: an overview. Microbiology. 2009. V. 155. Р.3476–3490. DOI: https://doi.org/10.1099/mic.0.032508-0
- MacIntyre H.L., Kana T.M., Anning T., Geider R.J. Photoacclimation of photosynthesis irradiance response curves and photosynthetic pigments in microalgae and cyanobacteria. Journal of Phycology. 2002. V. 38. P. 17–38. DOI: https://doi.org/10.1046/j.1529-8817.2002.00094.x
- Maksimovich G.A. Fundamentals of karst science. Questions of karst morphology, speleology and hydrogeology of karst. Permskoe Knizhnoe Izdatel'stvo, Perm', 1963. Т.1. 445 p. (In Russ.)
- Mandić M., Mihevc A., Leis A., Krajcar Bronić I. Concentration and stable carbon isotopic composition of CO2 in cave air of Postojnska jama, Slovenia. International Journal of Speleology. 2013. V. 42, №3. P. 279–287. DOI: http://doi.org/10.5038/1827-806X.42.3.11
- Martinez A., Asencio A.D. Distribution of Cyanobacteria at the Gelada Cave (Spain) by physical parameters. Journal of Cave and Karst Studies. 2010. V. 72, №. 1. P. 11–20. DOI: 10.4311/jcks2009lsc0082
- Martinčič A., Vrhovšek D., Batič F. Flora v jamah z umetno osvetlitvijo. Biološki Vestnik. 1981. V. 29, № 2. P.27–56.
- Matantseva O.V., Skarlato S.O. Mixotrophy in microorganisms: ecological and cytophysiological aspects. Journal of evolutionary biochemistry and physiology. 2013. V. 49, № 4. P. 377–388. DOI: https://doi.org/10.1134/S0022093013040014
- Mattey D.P., Atkinson T.C., Barker J.A., Fisher R., Latin J.-P., Durell R., Ainsworth M. Carbon dioxide, ground air and carbon cycling in Gibraltar karst. Geochimica et Cosmochimica Acta. 2016. V. 184. Р. 88–113. DOI: https://doi.org/10.1016/j.gca.2016.01.041
- Mazina S.E. Communities of photosynthetic organisms developing under artificial lighting conditions in the equipped area of the Marble cave. Speleologіya і karstologіya. 2009. №2. P. 92–99. (In Russ.)
- Mazina S.E. Lampenflora of Novoafonskaya cave. Politematicheskij setevoj elektronnyj nauchnyj zhurnal Kubanskogo gosudarstvennogo agrarnogo universiteta. 2015. V.9, № 113. P. 1–12. (In Russ.)
- Mazina S.E., Koncevova A.A., Yuzbekov A.K. Photosynthetic species of the Novoafonskaya cave, developing under artificial lighting conditions. Estestvennye i tekhnicheskie nauki. 2015. V.88, №10. P. 162–171. (In Russ.)
- Mazina S.E., Maksimov V.N. Photosynthetic organism communities of the Akhshtyrskaya excursion cave. Moscow University Biological Sciences Bulletin. 2011. V. 66. P. 37–41. DOI: https://doi.org/10.3103/S009639251101007X
- Mazina S.E., Semikolennyh A.A. Formation of soil-like bodies in artificial lighting areas in caves. In: Proceedings of the Int. scientific conf. The role of soils in the biosphere and human life. To mark the 100th anniversary of the birth of Academ. G.V. Dobrovolsky, the Intern. Year of Soils. MAKS Press, Moscow, 2015. P. 205–207. (In Russ.)
- McQuoid M.R., Hobson L.A. Review: diatom resting stages. Journal of Phycology. 1996. V. 32. P. 889–902. DOI: https://doi.org/10.1111/j.0022-3646.1996.00889.x
- Miskiewicz E., Ivanov A.G., Williams J.P., Khan M.U., Falk S., Huner N.P.A. Photosynthetic acclimation of the filamentous cyanobacterium, Plectonema boryanum UTEX 485 to temperature and light. Plant Cell Physiology. 2000. V.41, №6. P. 767–775. DOI: https://doi.org/10.1093/pcp/41.6.767
- Mulec J., Kosi G. Algae in the aerophytic habitat of Račiške ponikve cave (Slovenia). Natura Sloveniae. 2008. V.10, №1. P. 39–49. DOI: https://doi.org/10.14720/ns.10.1.39-49
- Mulec J., Kosi G. Lampenflora algae and methods of growth control. Journal of Cave and Karst Studies. 2009. V.71, №2. P 109–115.
- Mulec J., Kosi G., Vrhovsˇek D. Characterization of cave aerophytic algae communities and effects of irradiance levels on production of pigments. Journal of Cave and Karst Studies. 2008. V.70, №1. P. 3–12.
- Mulec J., Kubešová S. Diversity of bryophytes in show caves in Slovenia and relation to light intensities. Acta Carsologica. 2010. V.39, №3. P.587–596. DOI: https://doi.org/10.3986/ac.v39i3.86
- Murphy A.M., Cowles T.J. Effects of darkness on multiexcitation in vivo fluorescence and survival in a marine diatom. Limnology & Oceanography. 1997. V.42, №6. P. 1444–1453. DOI: https://doi.org/10.4319/lo.1997.42.6.1444
- Northup D.E., Lavoie K.H. Geomicrobiology of Caves: A Review. Geomicrobiology Journal. 2001. V.18(3). P. 199–222. DOI: https://doi.org/10.1080/01490450152467750
- Opsahl S.P., Chanton J.P. Isotopic evidence for methane-based chemosynthesis in the Upper Floridan aquifer food web. Oecologia. 2006. V.150, №1. P. 89–96. DOI: 10.1007/s00442-006-0492-2
- Palik P. A barlangok algavilágáról (Study into the algal flora of caves). Hidrológiai Közlöny. 1960. V. 40. P. 417–422.
- Palmer A.N. Origin and morphology of limestone caves. Geological Society of America Bulletin. 1991. V. 103. Р.1–21.
- Patrick R. Factors effecting the distribution of diatoms. The Botanical Review. 1948. V. 14. P. 473–524.
- Pattanaik B., Schumann R., Karsten U. Effects of ultraviolet radiation on cyanobacteria and their protective mechanisms. In: Seckbach J. (Ed.) Algae and cyanobacteria in extreme environments. – Springer, Dordrecht, 2007. – P. 29–45. DOI: https://doi.org/10.1007/978-1-4020-6112-7_2
- Pentecost A., Zhaohui Z. The distribution of plants in Scoska Cave, North Yorkshire, and their relationship to light intensity. International Journal of Speleology. 2001. V.30, №1. P. 27–37.
- Petersen J.B. The aërial Algae of Iceland. In: Rosenvinge L.K. & Warming E. (Eds.). The Botany of Iceland. J. Frimodt, Copenhagen, 1928. V. 2, №8. P. 325–447.
- Pfendler S., Karimi B., Maron P.-A., Ciadamidaro L., Valot B., Bousta F., Alaoui-Sosse L., Alaoui-Sosse B., Aleya L. Biofilm biodiversity in French and Swiss show caves using the metabarcoding approach: First data. Science of the Total Environment. 2018. V. 615. P. 1207–1217. DOI: https://doi.org/10.1016/j.scitotenv.2017.10.054
- Popović S., Simić G.S., Stupar M., Unković N., Jovanović J., Grbić M.L. Cyanobacteria, algae and microfungi present in biofilm from Božana Cave (Serbia). International Journal of Speleology. 2015. V. 44(2). P. 141–149. DOI: http://doi.org/10.5038/1827-806X.44.2.4
- Porter M.L., Engel A.S., Kinkle B., Kane T.C. Productivity-diversity relationships from chemolithoautotrophically based sulfidic karst systems. Int J Speleol. 2009. V. 38. P. 27–40. DOI: http://doi.org/10.5038/1827-806X.38.1.4
- Poulíčková A., Hašler P. Aerophytic diatoms from caves in central Moravia (Czech Republic). Preslia. 2007. V.79. P.185–204.
- Poulson T.L., White W.B. The Cave Environment // Science. 1969. V.165, №3897. Р.971–981. DOI: 10.1126/science.165.3897.971
- Puglisi M., Privitera M., Minissale P., Costa R. Diversity and ecology of the bryophytes in the cave environment: a study on the volcanic and karstic caves of Sicily. Plant Biosystems–An International Journal Dealing with all Aspects of Plant Biology. 2019. V.153, №1. P. 134–146. DOI: https://doi.org/10.1080/11263504.2018.1478903
- Raboy B., Padan E. Active transport of glucose and alpha-methyglucoside in cyanobacterium Plectonema boryanum. Journal of Biological Chemistry. 1978. V.253(9). P. 3287–3291.
- Racovitza E.G. Éssai sur les problèmes biospéleologiques. Arch. Zool. Exp. Générale. 1907. V.6. P. 371–488.
- Reinoso F.J., Viera Benitez M.C., Rodriguez O.J. Precisions on the ecology and chorology of Schistostega pennata (Hedw.) Webb & Mohr. in the Iberian Peninsula. Lazaroa. 1994. V.14. P. 13–19.
- Rajczy M. The flora of Hungarian caves. Karszt és Barlang. (Spec. issue). Budapest. 1989. Р. 69–72.
- Rengefors K., Anderson D.M. Environmental and endogenous regulation of cyst germination in two freshwater dinoflagellates. Journal of Phycology. 1998. V. 34(3). P. 568–577. DOI: https://doi.org/10.1046/j.1529-8817.1998.340568.x
- Roldán M., Clavero E., Canals T., Gómez-Bolea A., Ariño X., Hernández-Mariné M. Distribution of phototrophic biofilms in cavities (Garraf, Spain). Nova Hedwigia. 2004. V.78. P. 329–351. DOI: 10.1127/0029-5035/2004/0078-0329
- Roldán M., Hernández-Mariné M. Exploring the secrets of the three-dimensional architecture of phototrophic biofilms in caves. International Journal of Speleology. 2009. V.38, №1. P. 41–53. DOI: http://doi.org/10.5038/1827-806X.38.1.5
- Rother J.A., Fay P. Sporulation and the development of planktonic blue-green algae in two Salopian meres. Proceedings of the Royal Society of London, Series B: Biological Science. 1977. V.196 (1124). P. 317–332. DOI: https://doi.org/10.1098/rspb.1977.0043
- Sarbu S.M., Kane T.C., Kinkle B.K. A chemoautotrophically based cave ecosystem. Science. 1996. V.272 (5270). Р. 1953–1955. DOI: 10.1126/science.272.5270.1953
- Selvi B., Altuner Z. Algae of Ballıca Cave (Tokat-Turkey). International Journal of Natural and Engineering Sciences. 2007. V.1, №3. P.99–103.
- Semikolennykh A.A., Targulian V.O. Soil-like bodies of autochemolithotrophic ecosystems in the caves of the Kugitangtau Ridge, eastern Turkmenistan. Eurasian Soil Science. 2010. V. 43. P. 614–627. DOI: doi.org/10.1134/S1064229310060025
- Sharipova M. Yu., Dubovik I.Е. Cyanobacteria and Algae in the Karlamanskaya Cave (Bashkortostan Republic, Russia). Theoretical and Applied Ecology. 2024. No. 1. P. 184-190. DOI: 10.25750/1995-4301-2024-1-184-190 (In Russ.)
- Sherbenesku M., Deku V. A Study of the Cave Algae of Oltenia. Rev. Biol. 1962. V.7, №2. P. 201–214.
- Sicko-Goad L., Stoermer E.F., Kociolek J.P. Diatom resting cell rejuvenation and formation: time course, species records and distribution. Journal of Plankton Research. 1989. V.11(2). P. 375–389. DOI: https://doi.org/10.1093/plankt/11.2.375
- Šmarda J. Flóra kolem jeskynních reflektorů. In: Absolon K. Moravský kras. II. Academia, Praha, 1970. P. 304–305. (In Czech)
- Smith J.K.P., Hughes A.D., McEvoy L., Day J.D. Tailoring of the biochemical profiles of microalgae by employing mixotrophic cultivation. Bioresource Technology Reports. 2020. V.9. ID 100321. DOI: https://doi.org/10.1016/j.biteb.2019.100321
- Smith T., Olson R. A taxonomic survey of lamp flora (Algae and Cyanobacteria) in electrically lit passages within Mammoth Cave National Park, Kentucky. International Journal of Speleology. 2007. V.36, №2. P.105–114. DOI: http://doi.org/10.5038/1827-806X.36.2.6
- Souffreau C., Vanormelingen P., Verleyen E., Sabbe K., Vyverman W. Tolerance of benthic diatoms from temperate aquatic and terrestrial habitats to experimental desiccation and temperature stress. Phycologia. 2010. V.49. P. 309–324. DOI: https://doi.org/10.2216/09-30.1
- St. Clair L.L., Rushforth S.R., Allen J.V. Diatoms of Oregon Caves National Monument, Oregon. Great Basin Naturalist. 1981. V.41 (3). P. 317–332.
- St. Clair L.L., Rushforth S.R. The diatoms of Timpanogos Cave National Monument, Utah. American Journal of Botany. 1976. V.63 (1). P. 49–59. DOI: https://doi.org/10.1002/j.1537-2197.1976.tb11784.x
- Stal L.J. Cyanobacterial mats and stromatolites. In: Whitton B.A. & Potts M. (Eds.) The Ecology of the Cyanobacteria: Their Diversity in Space and Time. Dordrecht, Kluwer Academic Publishers, 2000. P.61–120.
- Thatcher E.P. Bryophytes of an artificially illuminated cave. Bryologist. 1949. V.52. P. 212–214.
- Tilzer M.M., Paerl H.W., Goldman C.R. Sustained viability of aphotic phytoplankton in Lake Tahoe (California-Nevada). Limnology & Oceanography. 1977. V.22. P. 84–91.
- Uher B., Kováčik L. Epilithic cyanobacteria of subaerial habitats in National Park Slovak Paradise (1998–2000). Bull. Slov. Bot. Spoločn., Bratislava. 2002. V.24. P. 25–29.
- Vinogradova O.N., Kovalenko O.V., Vasser S.P., Nevo E.D., Vajnshtejn-Evron M. Blue-green algae (Cyanoprocaryota) of Jamal Cave (Mount Carmel National Park, Israel). Algology. 2000. V.10, №1. P. 82–90. (In Russ.)
- Vinogradova O.N., Mikhajljuk T.I. Algal flora of caves and grottoes in the National Nature Park, "Podilsky Tovtry" (Ukraine). Algology. 2009. V. 19, № 2. P. 155–171. (In Russ.)
- Vinogradova O.N., Nevo E., Vasser C.V. Algoflora of the Sefunim Cave (Israel): species diversity under multifactorial abiotic stress. Algology. 2009. V. 19, № 1. P. 47–65. (In Russ.)
- Whitton B.A., Potts M. The ecology of cyanobacteria: their diversity in time and space. Kluwer Academic Publishers, Dordrecht, London, Boston, 2000. 669 p.
- Yentsch C.S., Reichert C.A. The effects of prolonged darkness on photosynthesis, respiration, and chlorophyll in the marine flagellate, Dunaliella euchlora. Limnology & Oceanography. 1963. V.8 (3). P. 338–342. DOI: https://doi.org/10.4319/lo.1963.8.3.0338
- Young E., Beardall J. Transient perturbations in chlorophyll a fluorescence elicited by nitrogen re-supply to nitrogen-stressed microalgae: distinct responses to NO3 versus NH4. Journal of Phycology. 2003. V.39. P. 332–342.
- Zammit G., Billi D., Albertano P. The subaerophytic cyanobacterium Oculatella subterranea (Oscillatoriales, Cyanophyceae) gen. et sp. nov: a cytomorphological and molecular description. Euro J Phycol. 2012. V.47(4). P. 314–354. DOI: https://doi.org/10.1080/09670262.2012.717106
- Zammit G., Billi D., Shubert E., Kaštovský J., Albertano P. The biodiversity of subaerophytic phototrophic biofilms from Maltese hypogeal. Fottea. 2011. V.11 (1). P. 187–201. DOI: 10.5507/fot.2011.018
- Zhondareva Ya.D., Trenkenshu R.P. Mixotrophic growth of Tetraselmis viridis in axenic culture. Voprosy sovremennoi algologii (Issues of modern algology). 2024. № 1 (34). P. 21–28. URL: http://algology.ru/2097 (date: 10.02.2024). DOI: https://doi.org/10.33624/2311-0147-2024-1(34)-21-28; END: MULCZK (In Russ.)
Author
Popkova Anna V.
Orcid ID – https://orcid.org/0000-0002-2435-954X
RUDN University, Moscow, Russia
popkova_av@pfur.ru
ARTICLE LINK:
Popkova A.V. Ecological features and biodiversity of phototrophic organisms in karst caves. Voprosy sovremennoi algologii (Issues of modern algology). 2024. № 2–3 (35–36). P. 84–109. URL: http://algology.ru/2102
DOI - https://doi.org/10.33624/2311-0147-2024-2-3(35-36)-84-109; EDN – GANSCS
Dear colleagues! If you want to receive the version of the article in PDF format, write to the editor,please and we send it to you with pleasure for free.
Address - info@algology.ru
When reprinting a link to the site is required
На ГЛАВНУЮ
Карта сайта
К разделу ОБЗОРЫ, СТАТЬИ И КРАТКИЕ СООБЩЕНИЯ

|
 |
|

