|
|
|
|
«Экологическая физиология водных фототрофов» I Сабининские чтения 15 ноября - 29 декабря 2012 г. Изменение свойств питательной среды по мере роста культур микроводорослей
Спиркина Н.Е., Ипатова В.И., Дмитриева А.Г. Natalia E. Spirkina, Valentina I. Ipatova, Aida G. Dmitrieva
Московский Государственный Университет им. М. В. Ломоносова,
УДК: 57.047:574.34
Исследовано влияние фильтратов, полученных на разных фазах роста культур зеленых хлорококковых микроводорослей, на рост клеток тех же видов. Возможность водорослей расти на фильтратах зависит от фазы роста культуры, на которой он был получен. Наиболее благоприятными для роста культур были фильтраты, полученные до 10 суток роста. Такие фильтраты обладали большим питательным потенциалом и, скорее всего, содержали меньше метаболитов, способных ингибировать рост культуры. В фильтратах, выделенных в более поздние периоды, рост культур существенно замедлялся. Ключевые слова: микроводоросли; экзометаболиты; скорость роста; деление клеток.
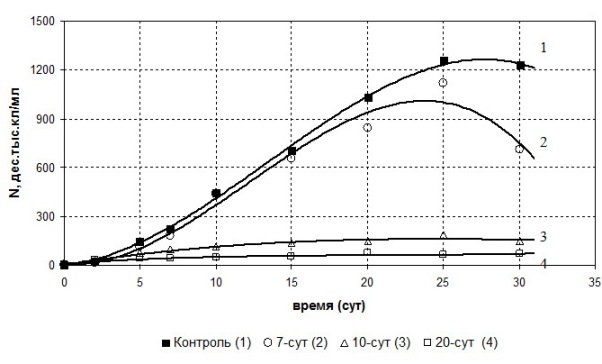
В результате своей жизнедеятельности водоросли изменяют состав жидкой питательной среды, на которой растут, обедняя ее минеральными веществами и выделяя в нее продукты обмена - экзометаболиты. Известно, что состав метаболитов зависит от видовой принадлежности водоросли, а также изменяется на протяжении жизни культуры. Показано, что большая часть органического вещества, выделяемого водорослями, приходится на долю соединений, не имеющих высокой биологической активности, к которым относятся продукты азотного и углеводного обмена. Кроме того, в составе экзометаболитов присутствуют физиологически активные вещества, которые могут как стимулировать, так и ингибировать деление клеток (Хайлов, 1971). Совокупность изменений, происходящих в составе питательной среды, отражается на ее способности поддерживать рост культур. Чтобы установить характер влияния этих изменений, была проведена серия экспериментов по исследованию роста двух видов водорослей в фильтратах культуральных сред, полученных на разных стадиях развития исходной культуры. Материалы и методы Объектами исследования послужили лабораторные культуры зеленых хлорококковых водорослей – Monoraphidium arcuatum (Korsch.) Hind. и Scenedesmus quadricauda (Turp.) Breb. M. arcuatum относится к одноклеточным водорослям, имеет форму полумесяца. Культура данного вида была выделена из пресноводного аквариума на кафедре гидробиологии МГУ им. М.В. Ломоносова в 2010 году. Sc. quadricauda – ценобиальная хлорококковая водоросль, в основном образующая ценобии по 2-4 клетки. Работы с данной культурой ведутся в лаборатории на протяжении многих лет. Культуры обоих видов выращивали на среде Успенского №1 (Успенская, 1966) с соблюдением стандартных условий в люминостате со сменой дня и ночи (12:12 ч) при досвечивании лампами дневного света и температуре 22±2ºС (Методика определения токсичности …, 2007). Для опыта отбирали однократно синхронизированные культуры водорослей, находившиеся в стадии логарифмического роста и содержавшие не менее 97% живых клеток (Методические указания …, 1998). Материалом для исследования служили бесклеточные фильтраты из 7, 10 и 20-суточных культур M. arcuatum и 7, 20 и 30-суточных культур Sc. quadricauda. Фильтрацию проводили с помощью водоструйного насоса через мембранный фильтр №5 отечественного производства. В полученный фильтрат, не разбавляя его чистой средой, инокулировали клетки того же вида, выращенные в отдельной культуре и в момент пересева находившиеся на логарифмической фазе роста и одновременно проводили посев тех же клеток в чистую среду в качестве контроля. Испытания проводили в пенициллиновых пузырьках объемом 10 мл. Численность клеток определяли в камере Горяева под световым микроскопом. Влияние фильтратов оценивали по их действию на изменение численности клеток в течение 30 суток, а также скорости деления клеток. Скорость деления клеток рассчитывали по формуле v=(lnN2-lnN1)/∆t, где N1 – численность клеток в культуре в момент времени t1, N2 - численность клеток в культуре в момент времени t2, ∆t – промежуток времени между t1 и t2. Дополнительно был проведен расчет увеличения численности на 30 сутки по отношению к исходной по формуле n=N30/N0, где N30 – численность на 30-е сутки роста, N0 – численность на нулевые (табл.1). Соотношение живых и мертвых клеток (Дмитриева, 1988) оценивали с помощью люминесцентного микроскопа Axioplan, Zeiss. Результаты и обсуждение Исследования показали, что фильтраты, полученные на разных фазах развития исходной культуры, в той или иной степени оказывали негативное влияние на рост водорослей. Так, численность клеток обоих видов в 7-суточных фильтратах изменялась в пределах контроля вплоть до 20 суток, после которых она начинала снижаться (рис.1 А,Б: кривая 2). Однако влияние фильтрата 10-суточной культуры M. arcuatum было иным: он ингибировал рост уже на начальных этапах, и на 6 сутки численность клеток была на 50% ниже, чем в контроле. Кривая роста в данном случае сильно отличалась от стандартной, которая обычно наблюдается в контроле (рис. 1 А: кривые 1,3). Такая же ситуация для этого вида наблюдалась и при выращивании в 20-суточном фильтрате, который оказывал еще большее ингибирующее действие на клетки (рис.1 А: кривая 4).
А
Б
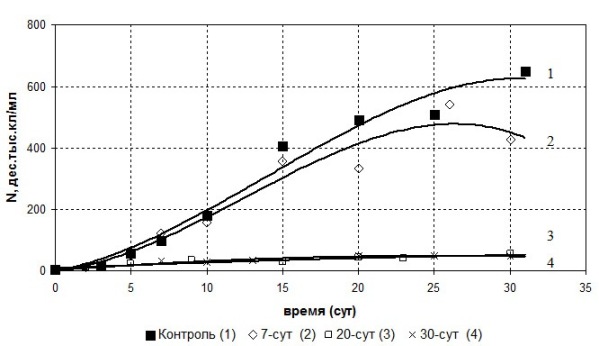
Рис.1. Изменение общей численности клеток в культурах Monoraphidium arcuatum (А) и Scenedesmus quadricauda (Б) при выращивании в чистой среде (1) и на фильтратах, выделенных в разные сроки роста культуры (2,3,4).
Рост культуры Sc. quadricauda в фильтратах проходил сходным образом (рис.1 Б). Дополнительно для этой культуры были проведены испытания 30-суточного фильтрата, показавшие, что он действовал на рост молодой популяции так же, как и 20-суточный - на рис.1 Б видно, что линии (3) и (4) практически полностью совпадают. Кроме того, для культур обоих видов при выращивании в фильтратах, полученных на 10, 20 и 30 сутки, было отмечено изменение морфологии клеток - они становились более крупными и бледными. Однако при этом клетки сохраняли фотосинтетическую активность, количество неактивных (отмирающих) клеток в этих повторностях не превышало 5%, как и в контроле. По данным литературы известно, что в период активного роста клетки могут образовывать антиоксидантные вещества, способные стимулировать их рост, а также бактерицидные вещества, подавляющие развитие бактериального компонента (Хайлов, 1971). В период седьмых суток роста, когда были получены первые фильтраты, исходные культуры обоих видов находились на логарифмической фазе роста, поэтому 7-суточные фильтраты могли содержать стимулирующие деление клеток вещества, но, с другой стороны, были уже истощены относительно исходной питательной среды. Снижение численности после двадцатых суток может быть объяснено, кроме того, совместным действием метаболитов, присутствовавших в фильтрате, а также метаболитов, выделенных в ходе роста на нем внесенной культуры. Характер роста культуры M. arcuatum в 10-суточном фильтрате был сходен с ростом в 20-суточном (рис.1 А), а рост культуры Sc. quadricauda в 20-ти суточном фильтрате – с ростом в 30-суточном. Вероятнее всего это связано с тем, что в период 10-20 и 20-30 суток у исходных культур отмечено снижение темпа деления клеток, что может быть связано как с накоплением в среде экзометаболитов, так и с образованием специфических веществ, ингибирующих деление. Кроме того, ранее было установлено (Спиркина и др., 2011), что замедление роста, которое происходит в культурах обоих видов к 10 суткам, связано с увеличением доли покоящихся клеток, не участвующих в делении. Можно предположить, что при попадании в 10- и 20-суточные фильтраты большая часть популяции M. arcuatum переходит в состояние покоя, так же как и клетки Sc. quadricauda при попадании в 20- и 30-суточные фильтраты. Отмеченное нами увеличения размеров клеток, скорее всего также является следствием присутствия в культуральной жидкости ингибирующих деление веществ. Под их влиянием клетки увеличиваются в размерах, готовясь к делению, которого не происходит. Таким образом, происходит торможение темпа деления клеток, что подтверждается данным таблицы (табл.). Подобный эффект был отмечен ранее для клеток Sc. quadricauda при интоксикации культуры (Прохоцкая, 2000).
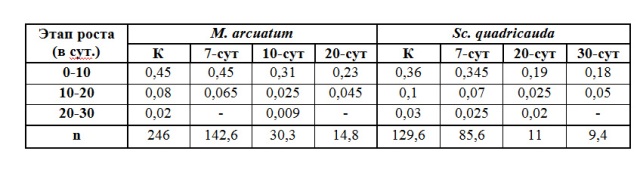
Таблица 1. Скорость деления клеток (кл/сут) в культурах Monoraphidium arcuatum и Scenedesmus quadricauda в контроле (К) и фильтратах, полученных на разных этапах роста (7-сут, 10-сут, 20-сут, 30-сут), и увеличение численности за 30 суток роста по отношению к исходной (n).
Из расчетных данных, представленных в таблице, следует, что для обоих видов водорослей при росте в фильтратах разного времени получения происходит снижение конечной численности относительно начальной, а также снижение скоростей роста. Так, наименьшая скорость роста была у обеих культур при росте на фильтратах, полученных после 20 суток. При развитии популяций обоих видов на 7-суточных фильтратах скорость роста изменялась в пределах контроля, однако отношение конечной численности к исходной (n) было снижено более, чем в 1,5 раза относительно контроля. Особенно сильное снижение данного показателя было отмечено при росте в 10, 20 и 30-суточных фильтратах. Резкое отличие скоростей деления клеток в период 0-10 от периода 10-20 суток в данных фильтратах свидетельствует о том, что популяции водорослей, попадая в условия недостатка питания и под воздействие ингибирующих веществ, тем не менее, проходят через характерные для развивающейся культуры стадии, которые, однако, выражено менее ярко.
В результате проведенного исследования нами были установлено следующее: 1. Возможность водорослей расти на фильтратах зависит от фазы роста культуры, на которой он был получен. Наиболее благоприятными для роста культур были фильтраты, полученные до 10 суток роста. Такие фильтраты обладали большим питательным потенциалом и, скорее всего, содержали меньше метаболитов, способных ингибировать рост культуры. В фильтратах, выделенных в более поздние периоды, рост культур существенно замедлялся. 2. При выращивании водорослей на фильтратах происходило снижение относительной численности клеток, сопровождаемое снижением темпа деления клеток. 3. Рост водорослей M. arcuatum и Sc. quadricauda при выращивании на их же фильтратах происходил сходным образом, что подтверждается данными об изменении численности клеток за 30 суток относительно контроля и скоростей их деления.
Список литературы 1. Дмитриева А.Г. Метод биотестирования по определению живых и мертвых клеток водорослей с помощью люминесцентной микроскопии // Методы биотестирования вод. Черноголовка, 1988. С. 85-89. 2. Методика определения токсичности вод, водных вытяжек из почв, осадков сточных вод и отходов по изменению уровня флуоресценции хлорофилла и численности клеток водорослей. М.: Акваросс, 2007. 48 с. 3. Методические указания по установлению эколого-рыбохозяйственных нормативов (ПДК и ОБУВ) загрязняющих веществ для воды водных объектов, имеющих рыбохозяйственное значение / Под ред. О.Ф. Филенко, С.А. Соколовой. М.: ВНИРО, 1998. 145 с. 4. Прохоцкая В.Ю. Структурно-функциональные характеристики популяции Scenedesmus quadricauda при интоксикации: Автореф. дисс. - М., 2000. - 22 с. 5. Спиркина Н.Е., Дмитриева А.Г., Ипатова В.И., Филенко О.Ф. Реакция хлорококковых водорослей на присутствие микроколичеств серебра // Антропогенное влияние на водные организмы и экосистемы: IV Всероссийская конференция по водной экотоксикологии, посвященной памяти Б.А. Флерова (Борок, 24-29 сентября 2011). - Ч.2. - С. 64-66. 6. Успенская В.И. Экология и физиология питания пресноводных водорослей. М.: МГУ, 1966. 124 с. 7. Экологическая физиология морских и планктонных водорослей (в условиях культур) / Под общ. редакцией К.М. Хайлова. Киев: Наукова Думка, 1971. 206 с. опубликовано - декабрь 2012 г.
Changes of the nutrient media properties during microalgae culturing Natalia E. Spirkina, Valentina I. Ipatova, Aida G. Dmitrieva The effect of the filtrate obtained in different phases of growth of the green microalgae, the growth of cells of the same species. Opportunity of the growth of algae on the filtrates depends on the phase of growth of the culture in which it was received. Most favorable for the algae were filtrates obtained up to 10 days of growth. These filtrates had more powerful nutritious potencial and contained fewer metabolites capable of inhibiting the growth of culture. In filtrates isolated in later periods, the algal growth was significantly slowed down. Keywords: microalgae; exometabolites; growth rate; cell division.
Об авторах Спиркина Наталья Евгеньевна - Spirkina Natalia Evgenievna аспирант natus25@list.ru Ипатова Валентина Ивановна - Ipatova Valentina Ivanovna кандидат биологических наук viipatova@hotmail.com Дмитриева Аида Георгиевна - Dmitrieva Aida Georgievna кандидат биологических наук aigdai@mail.ru Корреспондентский адрес: Россия, 119991, Москва, Ленинские горы, Московский Государственный Университет им.М.В.Ломоносова, д. 1, стр. 12, Биологический ф-т, каф. гидробиологии; тел.: (495) 939-11-48
ССЫЛКА НА СТАТЬЮ: Спиркина Н.Е., Ипатова В.И., Дмитриева А.Г. Изменение свойств питательной среды по мере роста культур микроводорослей // Вопросы современной альгологии. 2012. № 2 (2). URL: http://algology.ru/128
При перепечатке ссылка на сайт обязательна

|
|||
|
| ||